Поиск по сайту
Наш блог
Это странная ситуация: вы соблюдали все меры предосторожности COVID-19 (вы почти все время дома), но, тем не менее, вы каким-то образом простудились. Вы можете задаться...
Как диетолог, я вижу, что многие причудливые диеты приходят в нашу жизнь и быстро исчезают из нее. Многие из них это скорее наказание, чем способ питаться правильно и влиять на...
Овес-это натуральное цельное зерно, богатое своего рода растворимой клетчаткой, которая может помочь вывести “плохой” низкий уровень холестерина ЛПНП из вашего организма....
Если вы принимаете витаминные и минеральные добавки в надежде укрепить свое здоровье, вы можете задаться вопросом: “Есть ли лучшее время дня для приема витаминов?”
Ты хочешь жить долго и счастливо. Возможно, ты мечтал об этом с детства. Хотя никакие реальные отношения не могут сравниться со сказочными фильмами, многие люди наслаждаются...
Приседания и выпады-типичные упражнения для укрепления мышц нижней части тела. Хотя они чрезвычайно распространены, они не могут быть безопасным вариантом для всех. Некоторые...

Ученые из Стэнфордского университета разработали программу предсказывающую смерть человека с высокой точностью.

Глава Минздрава РФ Вероника Скворцова опровергла сообщение о падении доходов медицинских работников в ближайшие годы. Она заявила об этом на встрече с журналистами ведущих...

Федеральная служба по надзору в сфере здравоохранения озвучила тревожную статистику. Она касаются увеличения риска острой кардиотоксичности и роста сопутствующих осложнений от...

Соответствующий законопроект внесен в палату на рассмотрение. Суть его заключается в нахождении одного из родителей в больничной палате бесплатно, в течении всего срока лечения...
Система RH
К редко встречающимся относят антигены, частота которых в популяции ниже 1 %. Таких антигенов насчитывают 23 (см. табл. 4.1 и 4.26): Сх, V, Ew, VS, СЕ, Dw, hrH, Goa, RN, RoHar, Bea, Evans, Tar, Ces, Craw, Riv, JAL, STEM, ¥PTT9 BARC, JAHK, HOFM и LOCR. Семнадцать из них описаны в предыдущих разделах как маркеры парциальных D-антигенов, варианты или сателлиты антигенов С, Е, V, VS и г/иоантигенов. Приводим антигены, не упоминавшиеся выше.
Веа (Rh36)
В литературе описаны 4 случая обнаружения антител анти-Веа (Davidsohn, Stern и соавт. [255], МсСгеагу и соавт. [469], Ducos и соавт. [цит. по 544], Clark и соавт. [Joint Cong. ISBT/AABB, 1990, 81]), явившихся причиной гемолитической болезни новорожденных. Носительницами анти-Веа-антител были Женщины CDe/CDe, cDe/cde и cDE/cde, чьи мужья были cde/cde.
Stern, Davidsohn и соавт. [628] получили аллоиммунные антитела анти-Веа, проиммунизировав 2 добровольцев (CDe/CDe и cde/cde) эритроцитами мужа одной из упомянутых выше женщин (миссис Berrens), у которой впервые были найдены анти-Веа-антитела. С помощью полученных сывороток исследовано более 25 тыс. доноров разных национальностей, но среди них не обнаружено носителей антигена Веа. Лишь 20 лет спустя, после того как МсСгеагу и соавт. [469] описали второй случай анти-Веа-антител, было выявлено несколько лиц Веа+.
Антиген Веа, как было установлено Race и Sanger [544], является частью системы Rh. Он присутствует у лиц с фенотипом (c)d(e)(f), у которых антигены с, е и f (се) слабо выражены. Обследование представителей 3 поколений 1 семьи показало, что генный комплекс, кодирующий фенотип (c)d(e)(f) Веа+, передается по наследству.
Антиген Веа встречается не у всех людей (c)d(e)(f). Часть лиц имеют фенотип (c)d(e)(f)Bea-, что указывает на возможность существования как минимум двух генов (c)d(e), один из которых кодирует выработку антигена Веа, а другой - нет.
Описан ген rL (cLowde) [475], обусловливающий низкую экспрессию антигенов с и е, но в отличие от гена Веанормальную экспрессию антигена f (се).
Craw (Rh43)
Антиген Craw (Crawford), обнаруженный в 1980 г. Cobb [230], встречается у негров с частотой ОД %. Он чаще присутствует у лиц с фенотипом Cdes, но имеются и исключения. До настоящего времени описан только 1 случай aHra-Craw-антител.
HOFM
Антиген HOFM описан в 1990 г. Hoffman и соавт. [351]. Антитела анти-HOFM явились причиной умеренной ГБН. Эритроциты HOFM+ характеризуются сниженной экспрессией антигена С; другие антигены Rh без изменений.
LOCK (Rh55)
Антиген LOCR обнаружен Coghlan и соавт. [231] в 1994 г. Носители антигена LOCR имеют уменьшенную экспрессию антигена с или е. В 3 обследованных семьях ген LOCR наследовался с гаплотипом cde.
Coghlan и Zelinski [232] исследовали хромосому 1 у 19 членов одной из этих семей и установили, что антиген LOCR является частью системы Rh.
JAL (Rh48)
Редко встречающийся антиген JAL найден и изучен Lomas [447] и Poole с со- л авт. [535] в 2 семьях. Этот антиген присутствует в эритроцитах европейцев, имеющих фенотип (C)D(e). У негров антиген JAL ассоциирован с фенотипом (c)D(e). Среди 90 ООО обследованных швейцарских доноров только 4 были JAL+.
JAHK (Rh53)
Green и соавт. [311] описали редко встречающийся антиген JAHK, выявляемый антителами, присутствующими в некоторых поливалентных сыворотках. Антиген JAHK официально признан как составная часть системы резус. Предполагается, что его продукция кодируется геном rG.
Daniels [245] нашел, что ген rG является аллелем гена се, в котором часть экзона 2 содержит эквивалентные сегменты гена D. Как полагает автор, аминокислотная последовательность, кодируемая геном rG, обусловливает продукцию антигена JAHK, который расположен на 2-й экстрацеллюлярной петле Rh-полипептида.
DАК (Rh54)
В 2003 г. Reid и соавт. [559] описали редко встречающийся антиген DAK, который присутствовал в 31 образце эритроцитов, содержащих парциальный антиген DIIIa, и в 5 образцах эритроцитов, содержащих антиген DOL. Антиген DAK выявляли также на эритроцитах с фенотипом RN (10 образцов) и эритроцитах, имеющих комбинацию антигенов STEM и S (1 образец). При других комбинациях антигенов резус антиген DAK отсутствовал. Реагирование с эритроцитами DIIIa и DOL было сильнее, чем с эритроцитами RN. Авторы пришли к выводу, что антиген DAK сильнее выражен на эритроцитах DIIIa и DOL, чем на эритроцитах RN. Антиген DAK, получивший номер ISBT Rh54, был обнаружен у 4 % доноров африканского происхождения, проживающих в Нью-Йорке.
Редкий антиген 01а обнаружен Kornstad [396]. Он встречается на эритроци-ах с ослабленной экспрессией антигенов С, с, е и Е и некоторым ослаблением антигена D. Антиген 01а получил обозначение как серия 700043 ISBT, однако вскоре было выяснено, что он не кодируется локусом RH и к системе Rh не относится (см. Система RHAG).
CENR (Rh56)
В 1998 г. Reid и соавт. [558] описали 2 образца комбинированных антител анти-Dw +aHTH-Rh32, которые не удавалось разделить перекрестной адсорбцией эритроцитами Dw+Rh32- и Dw-Rh32+.
В 2004 г. эти же авторы сообщили, что эритроциты больного с генотипом DCw(e)/D~, имевшего фенотип Rh:-23,-32 (не содержавшие антигенов Dw и Rh32), взаимодействовали с указанными комбинированными антителами. Антиген, открываемый ими, получил обозначение CeNR. Молекулярно-генетическое обследование CeNR-положительных лиц выявило новый гибридный гаплотип Ce(l-5)-D(6-10). Незадолго до этого было установлено, что этот гибридный ген кодирует также антиген Cw, экспрессия антигенов Сие ослаблена (Westhoff и соавт. [704]). В 2005 г. новый антиген, получивший название CENR, был включен в систему под номером Rh56 (Issitt [372]).
Как показали Beckers и соавт. [158, 160], Roulliac и соавт. [581, 582], аминокислотные замены, проявляющие себя в виде фенотипов DVa, Rh32+, Rh33+ и DBT, обусловлены конверсиями генов D и СЕ в экзонах 4 и 5. Они приводят к появлению на полипептидах RHD и RHCE цепей с новыми, необычными последовательностями аминокислот. Эти фрагменты белковых цепей иммуноген-ны и способны стимулировать образование специфически распознающих их антител. Детальное изучение специфичности антител с эритроцитами редких фенотипов позволило выявить качественные различия антигенов Dw, Rh32, Rh33 и CENR между собой.
В 1967 г. появилось сообщение Schmidt и соавт. [598], а вскоре и других авторов [151, 153, 338, 353, 404, 501, 638] о том, что эритроциты Rhnull имеют не только серологические, но и морфологические, а также функциональные нарушения.
^Клинические проявления в виде умеренной компенсированной анемии с характерными лабораторными показателями у лиц Rhnull, Rhmod, -D- и других фенотипов делеций получили название синдрома дефицита Rh-антигенов, или синдрома Rhnull.
При синдроме Rhnull эритроциты не двояковогнуты, как в норме, а имеют чашкообразную форму [638]. При этом наблюдают ретикулоцитоз [371, 492, 599] и повышенный уровень антигена i [599], свойственный эритроцитам новорожденных, что свидетельствует о выбросе в кровяное русло незрелых эритроцитов.
Синдром дефицита Rh-антигенов сопровождается также снижением концентрации гемоглобина, сывороточного гаптоглобина и гематокрита, увеличением концентрации сывороточного билирубина и фетального гемоглобина.
Осмотическая резистентность эритроцитов в пределах нормы или несколько снижена. Лизис эритроцитов Rhnu|1 in vitro предотвращается добавлением к
Трг-системе глюкозы. Электрофоретическая подвижность эритроцитов Rhnull не изменена [601].
Степень анемии широко варьирует у разных людей с дефицитом Rh, даже среди сибсов, унаследовавших одни и те же гены [492].
Продолжительность жизни эритроцитов Rhnull in vivo сокращена [598]. Время приживления эритроцитов Rhnull у лиц Rhnull составляло 14-36 дней [532], у лиц с обычным Rh-фенотипом - 48-56 дней [338], что существенно ниже нормы.
Тип наследования, регуляторный или аморфный, не сказывается на особенностях клинических проявлений. Синдром в равной степени наблюдают у лиц XX XQ и Щ [151, 1533, 338, 353, 411, 504, 601, 638], у некоторых из них клинические нарушения достигают средней тяжести [226].
Чаще всего дефицит Rh-антигенов ничем себя не проявляет, и его носители чувствуют себя здоровыми людьми. Issitt и Anstee [374] наблюдали мужчину Rhnull; его жена имела фенотип cde; двое детей были CcDee, что указывало на регуляторный тип Rh у этого мужчины. У 3 сибсов и 4 сводных братьев этого человека фенотипы Rh не отличались от обычных.
Авторы подчеркивают, что пациенту было 76 лет, когда впервые обнаружили, что он не содержит антигенов резус. Тот факт, что фенотип RhnulI не диагностировали столь длительное время, подтверждает бессимптомное течение гемолитической анемии, обусловленной дефицитом Rh-антигенов.
Клинически выраженные формы гемолитической анемии, обусловленные дефицитом Rh-антигенов, полностью излечиваются спленэктомией, которая, необходима лишь в редких случаях [601].
У больных Rh и, подвергнутых спленэктомии, а также у лиц, спленэктоми-рованных в связи с травмой селезенки, продолжительность приживления эритроцитов Rhnull не отличалась от времени приживления обычных эритроцитов. Аномалии в мембране эритроцитов Rh u, Rhmod и других Rh-делеций сами по себе не сказываются на продолжительности циркуляции этих клеток в кровяном русле. Укороченный срок их жизни объясняется тем, что они распознаются и затем разрушаются клетками селезенки. В организме, лишенном селезенки, разрушение Rh-дефицитных эритроцитов не происходит.
Локализация генов Х°г и XQ
При исследовании нескольких семей установлено, что модифицирующие гены Х°г и Xе, обусловливающие фенотипы Rhnull и Rhmod, не связаны с локусом RH [225,226, 244]. Далее была установлена локализация генов Х°г и X?.
Эксперименты Ridgwell и соавт. [565] с гибридизацией соматических клеток показали, что гены RHAG, кодирующие продукцию Rh-ассоциированного гликопротеина, расположены на хромосоме 6 и не связаны с генами RH, которые находятся на хромосоме 1. Однако Rh-полипептиды и Rh-гликопротеины представляют собой Rh-антигенную субстанцию только в совокупности. При отсутствии гликопротеинов, связанных с Rh-полипептидами, антигены Rh не экс-прессированы, как, например, при регуляторном (Х°г/Х°г) типе Rhnuir
Генетическая независимость локусов RHAG (Rh50) и RH, а также влияние первого на функцию второго позволили Cherif-Zahar и соавт. [213] высказать предположение: не являются ли гены Х°г и Xе мутантными формами гена Rh50, расположенного на хромосоме 6?
Примечание. Мутантные формы гена Rh50 обозначены символом Rh с цифрой 50, которая показывает мол. массу кодируемого Rh-гликопротеина. В данном случае Rh50 не следует отождествлять с Rh50, обозначающим антиген FPTT.
Указанные авторы [213] обследовали 5 человек RhnullH одного Rhmod. Из 5 Rh 4 были Х°г/Х% 5-й был r=/r=. Rh , имел тип Х^/Х^. У 4 Rh „и null mod null 1 Rhmod, имевших регуляторный тип X°r/X°r и XQ/XQ соответственно, обнаружены мутантные формы Rh50, включавшие различные нуклеотидные замещения. Только у человека r-/r= (Rhnull аморфного типа) транскрипт гена Rh50 был нормальным. При исследовании кДНК Rh50 в экспериментах с гибридизацией in situ было показано, что ген Rh50 расположен на хромосоме 6 в области pll-p21.1 [213].
Таким образом, имеются все основания полагать, что регуляторные по происхождению фенотипы Rh u и Rhmod обусловлены мутациями в локусе RHAG (Rh-ассоциированного гликопротеина).
Антитела, образующиеся у лиц RhnuU
Из 22 носителей Rhnull (пробандов и их родственников) 7 (30,2 %) содержали антиэритроцитарные антитела (см. табл. 4.24), что свидетельствует о весьма высокой частоте аллоиммунизации лиц, лишенных антигенов резус. Антитела имели аллоиммунный характер (беременности, трансфузии), за исключением одного случая спонтанных антител у мужчины - донора крови.
У 1 пробанда имелись антитела анти-С и анти-е, у 2 антитела были слабыми и не идентифицировались.
Важная деталь: 4 из 7 сывороток (пробанды 4, 8, 10 и 1 из 2 сестер 9-го) содержали антитела, реагирующие с эритроцитами всех фенотипов Rh, в том числе -D-/-D-: и других Rh-делеций, за исключением эритроцитов Rhnull. Эти антитела, подробно изученные Haber и соавт. [331] и Bar-Shany и соавт. [153], получили название anti-total-Rh, а выявляемый ими широко распространенный антиген был обозначен как Rh total (Rh29).
У родильниц Rhnull отмечены случаи умеренной и тяжелой ГБН, вызванной aHTH-Rh29-annn^aMH. Тяжелый случай успешно купирован обменными трансфузиями крови cde в течение первых 24 ч после рождения ребенка (Lubenko и соавт. [451]). В одном случае ГБН была связана с анти-Hr -антителами (Perez-Perez и соавт. [Am. J. Hematol., 1992, V. 40, P. 306]). °
По-видимому, иммунный ответ у лиц RhnuI1 ограничивается образованием ан-дател в; общим антигенам - Rh29 и Нго. Антитела к частным антигенам (С, е и др.) вырабатываются реже. ion иммунизации добровольцев эритроцитами Rhnull антител к веществу Rhnull получить не удалось. Известна лишь одно сообщение, свидетельствующее о возможности существования таких антител. McGinnis и соавт. [471, 472] нашли у 4 больных анемией антитела IgM и IgG, которые они назвали антипрекурсорными. Сыворотки реагировали только с эритроцитами RhnuI1. Со стандартными эритроцитами (не Rhnull) агглютинации не наблюдали, однако после обработки стандартных эритроцитов трипсином реакция все же происходила.
Повреждение других антигенов на эритроцитах Rhnull
В табл. 4.25 суммированы имеющиеся в литературе данные относительно изменения статуса некоторых групповых антигенов эритроцитов у людей с фенотипом Rhnull. В основном это касается антигенов S, s, U, LW, Fy и i.
Экспрессия антигенов S, s и, особенно, U на эритроцитах Rhnull существенно снижена. Как показали Schmidt и соавт. [598], почти половина сывороток анти-S, анти-s и анти-U не реагировали с эритроцитами Rhnull S, Rhnull s и RhnullU в антиглобулиновой пробе. В реакции солевой агглютинации эти образцы эритроцитов реагировали хорошо.
Таблица 4.25
Изменение экспрессии некоторых антигенов на эритроцитах Rhnu|
|
Фенотип |
Экспрессия антигенов |
|||||||
|
S |
S |
и |
LW |
Fy5 |
i |
Rh29 total |
D |
|
|
Rh 1 null |
1 |
1 |
| |
1 |
||||
|
Rh А mod |
н |
н |
н |
н |
н |
н |
н |
следы |
Примечание. { - экспрессия снижена, | - повышена, н - не изменена.
Race и Sanger [544] пришли к выводу, что связывание антител с указанными антигенами при фенотипе Rhnull слабее, чем в норме. Слабофиксированные антитела легко удаляются с поверхности эритроцитов в процессе их отмывания при постановке антиглобулиновой пробы. Этим и объясняются разные результаты, получаемые в антиглобулиновой пробе и реакции солевой агглютинации.
Антигены LWa, LWb, LWab и Fy5 в эритроцитах Rhnul] отсутствуют, так же как и антигены Rh-Hr. Гены LWn Fy расположены на хромосоме 1 рядом с локусом RH и, по-видимому, претерпевают те же изменения, что и гены резус. Отсутствие указанных антигенов наблюдали независимо от регуляторного (Х°г/Х°г) или аморфного (г=/г=) типа Rhnull.
Schmidt и соавт. [598] отметили повышенную экспрессию антигена i у жен-Шины Rhnull, больной анемией. Sturgeon [638] констатировал некоторое повышение экспрессии антигенов М и N при фенотипе RhnulI.
|j|Race и Sanger [544] исследовали эритроциты 5 лиц Rhnull двумя сериями сывороток анти-Епа и установили, что эритроциты Rhnull Еп(а+) реагируют значительно
Сййьнее, чем эритроциты Еп(а+) обычных людей. Указанные авторы отметили также повышение экспрессии антигенов Kidd и Dombrock на клетках Rhn |
Природа дефицита некоторых антигенов на эритроцитах Rhn | понемногу проясняется. Установлено (Dahr и соавт. [241]), что эритроциты Rh н обоих генетических типов содержат 30-40 % гликофорина В (структура, которая несет на себе детерминанты S, s и U), т. е. в 2-3 раза меньше, чем эритроциты U+ с нормальным фенотипом Rh. Дефицит антигенов LW на эритроцитах Rhnull обусловлен отсутствием в их мембране соответствующего LW-гликопротеина (Bloy и соавт. [173]).
В отличие от фенотипа Rh $ при котором все антигены Rh отсутствуют, фенотип Rhmod (модифицированный) содержит небольшое, иногда исчезающее количество Rh-антигенов. Некоторые образцы эритроцитов, идентифицированные вначале как Rhnи, при более детальном исследовании оказывались Rhmod. Как показали Stevenson и соавт. [629], Rhnull - не всегда нуль.
Фенотип Rhmod появляется в результате воздействия на локус RH регулятор-ного (супрессорного) гена Xs. Этот ген, как полагают Chown и соавт. [225, 226], является аллелем геи&Х°г или самостоятельным геном, расположенным в ином, чем Х°г, локусе, регулирующем количество Rh-субстанции.
Семейные исследования подтвердили, что лица с фенотипом Rh, имеют нормальные гены RH [225, 226]. Таким образом, генетическая основа Rh ^ всегда регуляторного типа, в отличие от Rhnull, который может быть обусловлен аморфным типом наследования.
Количество антигенов Rh на эритроцитах лиц Rhmod значительно варьирует. В одних случаях Rh-антигены выявляют прямой реакцией агглютинации, в других -только с помощью высокочувствительного метода адсорбции - элюции. Mallory и соавт. [Vox. Sang., 1976, V. 30, R 430] нашли, что исследованные ими образцы эритроцитов Rhmod содержат только 1,2 % ожидаемого количества D-антигена.
Содержание гликофорина В на эритроцитах Rhmod уменьшено до 70 % от нормы.
Различают 2 типа Rh ull: регуляторный (супрессорный) и аморфный (отсутствие генетического материала).
Регуляторный тип формируется в результате взаимодействия генов RH, производящих соответствующие полипептиды, и генов Х]г, Х°г, которые управляют функцией локуса RH. Ген Х1г (доминантный) запускает нормальную продукцию Rh-полипептидов, а его редкий аллель Х°г (рецессивный) блокирует их синтез.
Ген Х]г широко распространен, поэтому большинство людей являются гомозиготами - Xlr/Xlr. При таком генотипе унаследованные от родителей гены RH функционируют нормально. При гетерозиготном варианте (Xlr/X°r) экспрессия антигенов, по данным одних авторов, не нарушена [331, 532], по данным других - снижена [353].
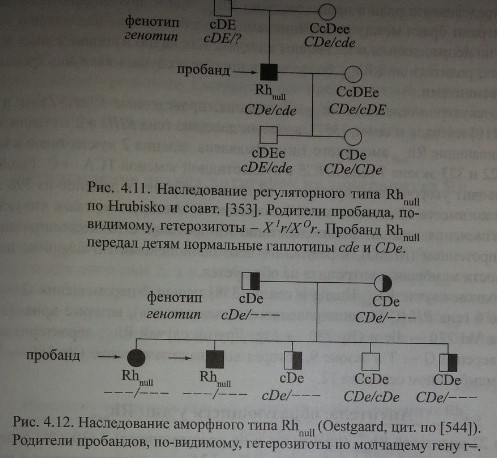
У людей, гомозиготных по супрессорному гену, Х°г/Х°г, присутствующие ДЯ-гены не функционируют. На рис. 4.11 представлен пример наследования ре-гуляторного типа Rh 1Г.
Аморфный тип Rhnull обусловлен отсутствием генетического материала, кодирующего продукцию Rh-полипептидов, по-видимому, вследствие делеции.
Получены данные, которые можно трактовать в пользу существования молчащего гена щ [371]. Пример наследования аморфного типа Rhnull представлен на рисунке 4.12. Родители пробандов - сибсы. Их фенотипы cDe и CDe создают видимость гомозиготности по генам с и С.
Судя по фенотипу детей, оба родителя были гетерозиготами: один, вероятно, cDe/r~> второй i CDe/r^. Двое детей имели одинаковый генотип г=/г=. Трое
других детей имели генотипы cDe/r=, CDe/r= и CDe/cDe. В приведенном примере недостает представителей третьего поколения, фенотипы которых могли бы подтвердить, что от родителей с аморфным типом Rhnul возможно рождение детей с таким же аморфным типом.
Обследование малого числа поколений в семьях не позволяет идентифицировать аморфный тип Rhnull, поскольку трудно получить убедительные доказательства того, что конкретный обследуемый человек генетически r=/r=, а не Х°г/Х°г. Генотип Х'г/Х°г также может приводить к уменьшению экспрессии антигенов Rh. Однако совокупность фактов, полученных при обследовании большого количества семей, позволила исследователям сделать вывод, что наследование Rhnull через молчащий ген г= вполне возможно.
Из 14 обладателей фенотипа Rhnull (см. табл. 4.24) у 9 был обнаружен регуля-торный тип Rhnull, у 3 - аморфный, у 2 - тип Rhnull не установлен.
Среди упомянутых выше 33 обследованных лиц Rh „ 20 имели регулятор-ный тип, 3 - аморфный тип, у остальных 10 человек генетическую основу нулевого фенотипа установить не удалось. Последующие многочисленные исследования подтвердили, что оба типа, регуляторный и аморфный, встречаются крайне редко, причем один из них, регуляторный, преобладает [151, 153, 331, 353, 532]. В некоторых случаях семейные исследования не могли выявить генетическую основу фенотипа Rhnull [501,647].
Определенную роль в происхождении Rhnull, как и других фенотипов делеций, играют браки между родственниками, способствующие накоплению гомозигот по депрессивным и молчащим аллелям. Как видно из приведенных выше данных, родители лиц Rhnullболее чем в половине случаев являлись кровными родственниками.
Молекулярно-генетические исследования, проведенные Cherif-Zahar и соавт. [210] и Huang и соавт. [357], выявили делецию гена RHD и 2 мутации, обусловливающие Rhnull аморфного типа. Выявлена делеция 2 нуклеотидов в кодо-нах 322 и 323 экзона 7 гена RHCE с нуклеотидной заменой ТСА Щ С. Такой ген производит укороченный протеин - 10 трансмембранных доменов из 398 аминокислот вместо 12 доменов из 417 аминокислот. Авторы полагают, что указанные изменения мешают взаимодействию Rh-протеина с Rh-ассоциированным гликопротеином (RhAG), в результате чего полноценный Rh-комплекс на поверхности мембраны эритроцита не образуется.
В одном случае Rhnull Huang и соавт. [358] нашли 2 перемещения G —> А в экзоне 6 гена RHAG (ассоциированного гликопротеина), которые приводили к замене Val 270 —| Не и Gly 280 й Arg. Другой случай Rhnull характеризовался трансверсией G —» Т в экзоне 9, которая вызывала замещение Gly 380 —> Val в трансмембранном сегменте 12.
Новости медицины
Много миллионов человек в мире принимают статины, но исследования показывают, что только 55% из тех, кому рекомендуется принимать статины, принимают их. Это большая проблема, потому что исследования также показывают, что те из группы...
Связанное с беременностью высокое кровяное давление может привести к долгосрочным сердечным рискам, показывают новые исследования.
Кэролин Консия, столкнулась с более серьезными последствиями репрессий против назначения опиоидов, когда узнала, почему сын ее подруги покончил с собой в 2017 году.
Новое исследование показывает, что психические заболевания не являются фактором большинства массовых расстрелов или других видов массовых убийств.