Поиск по сайту
Наш блог
Это странная ситуация: вы соблюдали все меры предосторожности COVID-19 (вы почти все время дома), но, тем не менее, вы каким-то образом простудились. Вы можете задаться...
Как диетолог, я вижу, что многие причудливые диеты приходят в нашу жизнь и быстро исчезают из нее. Многие из них это скорее наказание, чем способ питаться правильно и влиять на...
Овес-это натуральное цельное зерно, богатое своего рода растворимой клетчаткой, которая может помочь вывести “плохой” низкий уровень холестерина ЛПНП из вашего организма....
Если вы принимаете витаминные и минеральные добавки в надежде укрепить свое здоровье, вы можете задаться вопросом: “Есть ли лучшее время дня для приема витаминов?”
Ты хочешь жить долго и счастливо. Возможно, ты мечтал об этом с детства. Хотя никакие реальные отношения не могут сравниться со сказочными фильмами, многие люди наслаждаются...
Приседания и выпады-типичные упражнения для укрепления мышц нижней части тела. Хотя они чрезвычайно распространены, они не могут быть безопасным вариантом для всех. Некоторые...

Ученые из Стэнфордского университета разработали программу предсказывающую смерть человека с высокой точностью.

Глава Минздрава РФ Вероника Скворцова опровергла сообщение о падении доходов медицинских работников в ближайшие годы. Она заявила об этом на встрече с журналистами ведущих...

Федеральная служба по надзору в сфере здравоохранения озвучила тревожную статистику. Она касаются увеличения риска острой кардиотоксичности и роста сопутствующих осложнений от...

Соответствующий законопроект внесен в палату на рассмотрение. Суть его заключается в нахождении одного из родителей в больничной палате бесплатно, в течении всего срока лечения...

Эритроциты А(П) с пониженными агглютйнационными свойствами впервые описали Dungem и Hirszfeld в 1911 г. [94]. Landsteiner и Levine [133] подразделили фенотип А на подгруппы.
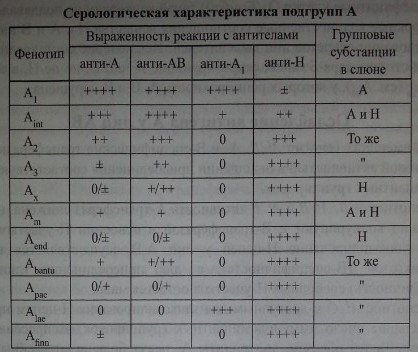
Около 88 % лиц группы А относятся к подгруппе А1 12 % - к подгруппе А^. Среди лиц AB(IV) 80 % Afi, 20 % А2В. Ранее полагали, что лица А1 имеют антигены А и Ар а лица А2 - только антиген А. Клетки и А2 несут различное количество антигенного вещества, имеющего в то же время и некоторые качественные отличия. Так, сыворотки анти-А лиц, имеющих группу крови В(111), содержат 2 фракции анти-А-антител: одна фракция (анти-А) реагирует с эритроцитами Aj и А2, другая (анти-Aj) - только с эритроцитами кх (Wiener и соавт. [225, 227]). Адсорбция сывороток анти-А эритроцитами А2 позволяет получить реактив, который не реагирует с эритроцитами А2, но сохраняет высокую активность по отношению к эритроцитам и может быть использован для дифференцировки образцов эритроцитов А на Аги А2(Р.М. Уринсон [61]).
Для определения подгрупп А используют экстраагглютинины и а2, специально отобранные моноклональные антитела анти-А, а также лектины Dolichos biflorus и Ulex europaeus. Первый из них реагирует с эритроцитами А1 второй - с эритроцитами А2.
У лиц Aj с частотой примерно 1 на 10 ООО встречаются экстраагглютинины о^. Лица А2 и А2В содержат экстраагглютинины cL с частотой 1 на 50 и 1 на 5 соответственно.
Гены А1 и А2 передаются по наследству. Лица А1 А2 имеют фенотип Аг
Возникновение 2 или более популяций эритроцитов, несущих различное количество А-эпитопов, обусловлено А-трансферазами, модифицировавши вирусами или сформировавшимися под влиянием атипичных 50-аллелей.
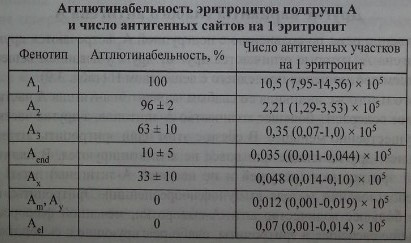
Агглютинационные свойства эритроцитов различных подгрупп А, а также число А-эпитопов весьма вариабельны.
Варианты антигена А получили индивидуальные названия, однако это не означает, что каждый их них представляет независимую генетически детерминированную подгруппу. Они скорее являются исключением из правил нормального формирования группового вещества.
Как уже отмечалось, большинство антител анти-А лиц группы В не агглютинирует эритроциты Ах. Сыворотки крови лиц В, иммунизированных групповым веществом А, напротив, обладают такой способностью. Моноклональные реагенты анти-А выявляют подгруппу Ах, однако в некоторых случаях эти тест- системы взаимодействуют также и с антигеном В.
Эритроциты Ах очень редки - 1 : 40 000-77 ООО (Reid, Lomas-Francis [186]).
Специфическая А-трансфераза обычно отсутствует в сыворотках крови и на эритроцитах лиц подгруппы А , активность Н-трансферазы снижена.
Результаты посемейных исследований противоречивы. В некоторых семьях удавалось проследить наследование подгруппы Ах как фенотипического проявления редкого аллеля А . В других семьях пробанды Ах имели родителей О (Beckers и соавт. [73], Valdes и соавт. [214], Van Loghem и соавт. [215]). Ducos и соавт. [93] наблюдали детей Ах в семьях, где один из родителей имел группу А2В.
Дифференцировать подгруппы А2/В и Ах/В можно по отсутствию в сыворотке крови лиц Ах/В A-специфической трансферазы.
Как отмечают Issitt и Anstee [122], некоторые производители моноклональных антител предъявляют повышенные требования к своим реактивам и используют для оценки их качества эритроциты А .
Вещества, вызывающие агглютинацию А-, В- или Н-положительных эритроцитов человека, были найдены во многих растениях, водорослях, грибах, а также в тканях некоторых червей, улиток, икре лососевых рыб, сыворотке крови угрей. Они были названы лектинами (табл. 3.6). Установлено, что они взаимодействуют с терминальными моносахаридными группировками. Лектины из Dolichos biflorus и Ulex europaeus используют для дифференцировки подгрупп А в исследовательских целях (П.Н. Косяков [35], Прокоп, Геллер [56], Daniels [87], Issitt, Anstee [122], Sringarm и соавт. [201]), в рутинной практике определения групп крови АВО их не применяют.
Таблица 3.6
Лектины с анти-А-, анти-В-, анти-AB- и анти-Н-активностью
|
Источник получения |
Специфичность |
|
|
Dolichos biflorus |
Семена |
Анти-А |
|
Phaseolus limensis |
To же |
Анти-А |
|
Phaseolus lunatus |
II |
То же |
|
Helix pomatia |
Печень |
II |
|
Helix hortensis |
To же |
II |
|
Fomes fometarius |
Мицелий |
АнпьВ |
|
Ptilota plumosa |
Органеллы |
То же |
|
Salmo salar |
Икра |
)1 |
|
Sophora japonica |
Семена |
Анти-АВ |
|
Phlomis Jructosa |
То же |
То же |
|
Bandeiraea simplicifolia |
II |
II |
|
Ulex europaeus |
II |
Анти-Н |
|
Lotus tetragonolous |
11 |
Анти-Н (HI) |
|
Anguilla anguilla |
Анти-Н (HI) |
|
|
Cystisus sessifolius |
Семена |
Анти-Н |
|
Laburnum alpinum |
То же |
То же |
Антиген С
Существование антигена С в системе АВО можно считать доказанным. Он содержится в эритроцитах А(П), В(Ш) и AB(IV). В эритроцитах 0(1) антиген С отсутствует.
Основанием для такого утверждения служат эксперименты Wiener и соавт. [213, 224, 228-230], показавшие, что сыворотки Оар(1), помимо а- и Р-агтлютининов, реагирующих с эритроцитами А и В, содержат еще одну разновидность естественных групповых антител - С-агтлютинины (по Винеру анти-С- антитела), которые реагируют с эритроцитами А и В перекрестно
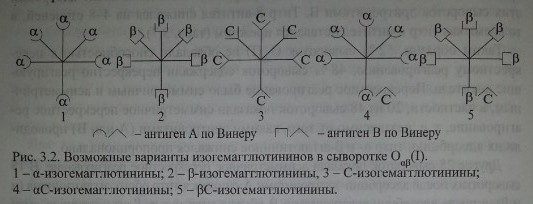
На наш взгляд, перекрестное реагирование обусловлено не ар-агглютининами, как полагала Dodd и соавт., а антителами аС, PC, что в большей мере согласуется с концепцией Винера, а также полученными нами данными. На рис. 3.2 представлена предполагаемая модель этих антител.
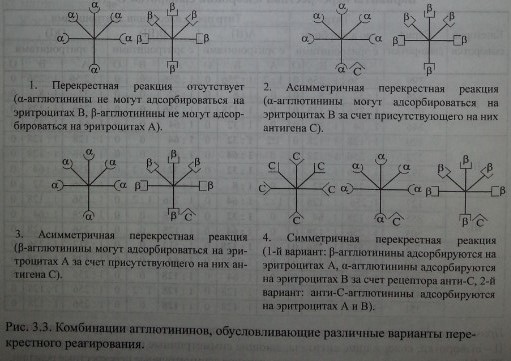
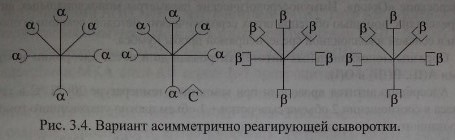
Представленная структурная модель изогемагглютининов позволяет объяснить характер перекрестного реагирования сывороток Оар(1). Сыворотки, не вызывающие перекрестных реакций, содержат только а- и (3-антитела (рис. 3.3, п. 1). Сыворотки, вызывающие симметричные перекрестные реакции, содержат, помимо а- и р-антител, антитела аС и PC или анти-С-антитела (рис. 3.3, п. 4). Сыворотки, вызывающие асимметричные перекрестные реакции, содержат а, р и одну из разновидностей антител - аС или PC (рис. 3.3, п. 2, 3).
Комбинации агглютининов, обусловливающие различные варианты перекрестного реагирования.
Вариант асимметрично реагирующей сыворотки.
Согласно схеме сыворотка содержит 50 % а-агглютининов, 75 % - р. Валентность анти-С реагирует как а и р. При адсорбции такой сыворотки эритроцитами А а-агглютинины будут удалены полностью. Иными словами, из сыворотки будет удалено 50 % антител. При адсорбции сыворотки эритроцитами В будет удалено 75 % антител (50 % Р+25 % а) за счет рецептора анти-С. В случае, если рецептор анти-С связан не с а-, а с р-агглютининами, асимметричное реагирование проявят эритроциты А, унося на своей поверхности 25 % Р-агглютининов.
Как далее нами показано, перекрестно реагирующие антитела так же, как иммунные антитела АВО и Rh, относятся к классу IgG, устойчивы к унитиолу, лучше реагируют с отмытыми, чем неотмытыми эритроцитами, в отличие от иммунных (термо- сгабильных) антител являются термолабильными (утрачивают активность после прогревания сыворотки при 70 °С в течение 10 мин). В противоположность классическим иммунным антителам IgG, которые адсорбируются на эритроцитах, но не вызывают их агглютинации, перекрестно реагирующие антитела непосредственно агглютинируют эритроциты в солевой среде. В низкой концентрации они утрачивают способность агглютинировать эритроциты, однако сенсибилизируют их подобно неполным антителам и хорошо выявляются в непрямой антиглобулиновой пробе Кумбса.
Сыворотки лиц 0^(1), очевидно, содержат несколько типов групповых антител: изогемагглютинины аир IgM, аир IgG, аС и рС IgG* анти-С IgG, иммунные аир IgM, иммунные а и Р IgG, что закономерно обусловливает перекрестные реакции с различными групповыми антигенами.
Важным аргументом, подтверждающим концепцию Винера о существовании антигена С, явились эксперименты по получению специфических антисьгворотк. В частности, при иммунизации мышей эритроцитами А(П) и В(Ш) нами [21] были получены моноклональные антитела со специфичностью анти-АВ (МКА-АВ). Материал и методы. Трехмесячным самкам мышей BALB/c вводили по 0,1 мл отмытых 0,9% NaCl эритроцитов А(П) или В(Ш) внутрибрюшинно дважды с интервалом в 7 дней. Третью инъекцию производили внутривенно за 5 дней до слияния спле- ноцитов с клетками миеломы NS-1. Слияние осуществляли по стандартной методике с использованием 45% полиэтиленгликоля-1500 «ЬоЬа» и 5% диметилсульфоксида.
Эффективность гибридизации составляла 10-5. Клонировали гибридные клетки в среде HAT без фидера. Антителопродуцирующие клоны отбирали с помощью реакции аг
в 96-луночных планшетах с отмытыми эритроцитами 0(1), А(П) и В(Щ), Класс моноклональных антител устанавливали по флюоресценции сенсибилизи-IgG, нейтрализовались группоспецифическими субстанциями, существенно отличает их от классических иммунных антител и позволяет выделить их в особую группу - иммунные IgG-антитела термолабильные легко нейтрализуемые. К этой же группе могут быть отнесены перекрестно реагирующие антитела лиц 0(1), имеющие идентичную иммуносерологическую характеристику - IgG термолабильные. Их происхождение (иммунное или естественное) остается неясным. Не исключено, что они так же, как МКА анти-АВ, являются иммунными.
Обработка эритроцитов В(Ш) протеолитическими ферментами, специфически разрушающими антиген В, лишала эритроциты групповых свойств. После такой обработки эритроциты В(Ш) в отличие от обработанных глутаровым альдегидом приобретали свойства эритроцитов 0(1) группы и не агглютинировались сыворотками анти-В. Одновременно исчезала их способность взаимодействовать с перекрестно реагирующими антителами МКА анти-АВ, а также перекрестно реагирующими антителами лиц 0(1).
По характеру реагирования полученные МКА анти-АВ вряд ли можно отнести к анти-А и анти-В. По-видимому, это одно, маскирующееся под анти-А и анти-В антитело, реагирующее с общей для эритроцитов А(П) и В(Ш) антигенной детерминантой. По своим свойствам эти антитела близки к перекрестно реагирующим антителам сывороток лиц 0(1), описанным выше. Сам факт получения антител анти-АВ в ответ на иммунизацию эритроцитами как А, так и В служит веским аргументом в пользу того, что оба антигена наряду с существенными серологическими различиями имеют идентичный эпитоп С, в равной мере являющийся сильным иммуногеном.
Таким образом, имеются все основания полагать, что групповая система АВО представлена не двумя агглютиногенами - А, В и двумя агглютининами - а, Р, а тремя агглютиногенами - А, В, С и тремя агглютининами - а, р и С.
Антиген С выявляют с помощью перекрестно реагирующих сывороток лиц Оар(1) [184, 229]. Именно фракция перекрестно реагирующих агглютининов представляет собой антитела анти-С. Последние можно удалить из сыворотки указанных лиц адсорбцией как А, так и В эритроцитами. При рутинном исследовании антиген С маскируется присутствием антигена А и/или В. Антитела анти-С в обычных методах исследования проявляют себя подобно несепари- руемой комбинации а- и Р-агглютининов. У лиц, имеющих группу крови А и В, агглютинины анти-С отсутствуют.
Не исключено, что антитела анти-С могут встречаться в чистом виде. Однако отличить их от анти-А и анти-В обычными методами не представляется возможным. У плодов 0(1) от матерей 0(1) находят антитела со свойствами анти-С, у плодов А(Н) и В(Ш) от матерей А(Н) и В(Ш) таких антител не находят.
Owen (цит. по Wiener [229]) получил чистую фракцию анти-С-агглютининов адсорбцией сывороток 0^(1) эритроцитами опоссума и кролика, которые, содержат парциальный антиген В и, по-видимому, не содержат антигена С. После такой обработки оставшиеся в сыворотке антитела анти-С реагировали с эритроцитами А и В, и их можно было удалить эритроцитами А или В в ад- <юрбционной пробе. Однако для окончательного доказательства того, что С-, о- и Р-агглютинины являются самостоятельными независимыми друг от друга антителами, не достает эксперимента, в котором антигены А и В были бы разрушены ферментативно (не реагировали бы с сыворотками анти-А и анти-В), но при этом сохранили бы антиген С (продолжали бы агглютинироваться анти-С- сывороткой или элюатом аР). Только в том случае, если эритроциты не агглютинируются а и р, но продолжают агглютинироваться анти-С-антителами, можно не только с достаточной степенью уверенности констатировать существование антигена С, но и с помощью такого реактива изучить закономерности наследования этого антигена, возможные его разновидности и комбинации. В наших экспериментах ферментативное разрушение В-антигена приводило одновременно к утрате их способности реагировать с МКА анти-АВ. Иными слова ми разрушение В-антигена влекло за собой разрушение антигена С. Однако, не смотря на отрицательный результат этого эксперимента, полученные нами данные в целом со всей очевидностью свидетельствуют о наличии третьего антигена в системе АВО, существование которого блестяще предсказал Wiener. глютинации
Изогемагглютинины анти-А и анти-В отсутствуют в крайне редких случаях: у больных врожденной гипо- и агаммаглобулинемией, а также при Х-ассоциированном синдроме Вискотта - Олдриджа. Такие лица не способны синтезировать антитела к полисахаридным, но не белковым антигенам.
Изогемагглютинины отсутствуют при истинном химеризме, наблюдаемом у ди- зиготных близнецов. В период внутриутробного развития между близнецами может происходить обмен кроветворными клетками, в результате чего после рождения у каждого из близнецов в кровотоке присутствуют 2 популяции эритроцитов с различными фенотипами. Описаны химеры, когда 90 % циркулирующих эритроцитов имели группу О, а остальные 10 % - группу А. У таких индивидов в плазме крови обнаруживали только анти-В-антитела, анти-А отсутствовали (см. Кровяные химеры).
В очень редких случаях изогемагглютинины отсутствовали у здоровых лиц без признаков гипогаммаглобулинемии или какой-либо другой патологии. По данным Dobson и Ikin, изогемагглютинины отсутствовали у 0,01 % здоровых лиц. Авторы связывали это с соматическими мутациями, приводящими к инактивации клонов В-клеток, запрограммированных на синтез соответствующих антител. Интересно, что родители, братья и сестры пробандов содержали изогемагглютинины, характерные для соответствующей группы крови. Возможно, синтез АВО-антител контролируется широко встречающимся доминантным геном и его редко встречающимся рецессивным молчащим аллелем. Лица без изогемагглютининов являются гомозиготными по указанному рецессивному аллелю.
Онтогенез АВО-антигенов
Подобно антителам, антигены системы АВО в момент рождения развиты не полностью, хотя у эмбрионов их обнаруживают уже на 5-й неделе внутриутробного развития. Эритроциты пуповинной крови реагируют с антителами анти-А и анти-В слабее по сравнению с клетками взрослых лиц (Witebsky и Engasser [97, 233], Romano и соавт. [187]). Эритроциты некоторых новорожденных группы А по своей агглютинабельности могут приближаться к эритроцитам А2. У 6-18-месячного ребенка агглютинабельности эритроцитов повышается, серологические характеристики соответствуют группе А,. Эритроциты новорожденных А, лучше реагируют с лектином Dolichos biflorus, чем с антителами анти-А, аллогенного происхождения. Эритроциты детей А2 более интенсивно взаимодействуют с антителами анти-А,В, чем с антителами анти-А, и тем самым показывают сходство с подгруппой Ах. Антиген Н на эритроцитах новорожденных выражен почти так же, как и у взрослых.
Эритроциты новорожденных А несут существенно меньшее количество А-антигенных участков (табл. 3.5) по сравнению с клетками взрослых лиц А, (Economidou и соавт. [95]). В то же время более высокая активность ^-трансферазы зарегистрирована в сыворотках пуповинной крови, чем в сыворотках крови взрослых.
Слабые реакции эритроцитов новорожденных с антителами анти-А и анти-В можно объяснить тем, что указанные антитела связываются с эритроцитами не двумя, а одним Fc-учаетком. На эритроцитах детей цепи, несущие антигены А и В, недостаточно разветвлены. По мере разветвления меняется пространственная конфигурация эпитопов, их количество увеличивается и они становятся доступнее для активных участков антител. Повышение агглютинабельных свойств эритроцитов происходит постепенно в течение первых 6-18 мес. жизни. Концентрация (31 —»6-глюкозаминилтрансферазы, участвующей в формировании разветвления, у новорожденных низкая. Содержание этого фермента достигает уровня его у взрослых в течение первых 6-18 мес. жизни.
Таблица 3.5
Плотность распределения А-антигена на эритроцитах
|
Группа крови |
Количество антигенных участков, тыс. на 1 эритроците |
|
|
новорожденных |
взрослых |
|
|
Ai . |
250-370 |
810-1170 |
|
А2 |
140 |
240-290 |
|
А,В |
220 |
460-850 |
|
а2в |
|
120 |
|
В |
|
610-830 |
Подобно антителам, антигены системы АВО в момент рождения развиты не полностью, хотя у эмбрионов их обнаруживают уже на 5-й неделе внутриутробного развития. Эритроциты пуповинной крови реагируют с антителами анти-А и анти-В слабее по сравнению с клетками взрослых лиц (Witebsky и Engasser, Romano и соавт. ). Эритроциты некоторых новорожденных группы А по своей агглютинабельности могут приближаться к эритроцитам А2. У 6-18-месячного ребенка агглютинабельности эритроцитов повышается, серологические характеристики соответствуют группе А,. Эритроциты новорожденных А, лучше реагируют с лектином Dolichos biflorus, чем с антителами анти-А, аллогенного происхождения. Эритроциты детей А2 более интенсивно взаимодействуют с антителами анти-А,В, чем с антителами анти-А, и тем самым показывают сходство с подгруппой Ах. Антиген Н на эритроцитах новорожденных выражен почти так же, как и у взрослых.
Эритроциты новорожденных А несут существенно меньшее количество А-антигенных участков (табл. 3.5) по сравнению с клетками взрослых лиц А, (Economidou и соавт.). В то же время более высокая активность ^-трансферазы зарегистрирована в сыворотках пуповинной крови, чем в сыворотках крови взрослых.
Слабые реакции эритроцитов новорожденных с антителами анти-А и анти-В можно объяснить тем, что указанные антитела связываются с эритроцитами не двумя, а одним Fc-учаетком. На эритроцитах детей цепи, несущие антигены А и В, недостаточно разветвлены. По мере разветвления меняется пространственная конфигурация эпитопов, их количество увеличивается и они становятся доступнее для активных участков антител. Повышение агглютинабельных свойств эритроцитов происходит постепенно в течение первых 6-18 мес. жизни. Концентрация (31 —»6-глюкозаминилтрансферазы, участвующей в формировании разветвления, у новорожденных низкая. Содержание этого фермента достигает уровня его у взрослых в течение первых 6-18 мес. жизни.
Таблица 3.5
Плотность распределения А-антигена на эритроцитах
|
Группа крови |
Количество антигенных участков, тыс. на 1 эритроците |
|
|
новорожденных |
взрослых |
|
|
Ai . |
250-370 |
810-1170 |
|
А2 |
140 |
240-290 |
|
А,В |
220 |
460-850 |
|
а2в |
|
120 |
|
В |
|
610-830 |
Лектины
Вещества, вызывающие агглютинацию А-, В- или Н-положительных эритроцитов человека, были найдены во многих растениях, водорослях, грибах, а также в тканях некоторых червей, улиток, икре лососевых рыб, сыворотке крови угрей. Они были названы лектинами (табл. 3.6). Установлено, что они взаимодействуют с терминальными моносахаридными группировками. Лектины из Dolichos biflorus и Ulex europaeus используют для дифференцировки подгрупп А в исследовательских целях (П.Н. Косяков [35], Прокоп, Геллер [56], Daniels [87], Issitt, Anstee [122], Sringarm и соавт. [201]), в рутинной практике определения групп крови АВО их не применяют.
Таблица 3.6
Лектины с анти-А-, анти-В-, анти-AB- и анти-Н-активностью
|
Источник получения |
Специфичность |
|
|
Dolichos biflorus |
Семена |
Анти-А |
|
Phaseolus limensis |
To же |
Анти-А |
|
Phaseolus lunatus |
II |
То же |
|
Helix pomatia |
Печень |
II |
|
Helix hortensis |
To же |
II |
|
Fomes fometarius |
Мицелий |
АнпьВ |
|
Ptilota plumosa |
Органеллы |
То же |
|
Salmo salar |
Икра |
)1 |
|
Sophora japonica |
Семена |
Анти-АВ |
|
Phlomis Jructosa |
То же |
То же |
|
Bandeiraea simplicifolia |
II |
II |
|
Ulex europaeus |
II |
Анти-Н |
|
Lotus tetragonolous |
11 |
Анти-Н (HI) |
|
Anguilla anguilla |
Анти-Н (HI) |
|
|
Cystisus sessifolius |
Семена |
Анти-Н |
|
Laburnum alpinum |
То же |
То же |
Изогемагглютинины анти-А и анти-В отсутствуют в крайне редких случаях: у больных врожденной гипо- и агаммаглобулинемией, а также при Х-ассоциированном синдроме Вискотта - Олдриджа. Такие лица не способны синтезировать антитела к полисахаридным, но не белковым антигенам.
Изогемагглютинины отсутствуют при истинном химеризме, наблюдаемом у ди- зиготных близнецов. В период внутриутробного развития между близнецами может происходить обмен кроветворными клетками, в результате чего после рождения у каждого из близнецов в кровотоке присутствуют 2 популяции эритроцитов с различными фенотипами. Описаны химеры, когда 90 % циркулирующих эритроцитов имели группу О, а остальные 10 % - группу А. У таких индивидов в плазме крови обнаруживали только анти-В-антитела, анти-А отсутствовали (см. Кровяные химеры).
В очень редких случаях изогемагглютинины отсутствовали у здоровых лиц без признаков гипогаммаглобулинемии или какой-либо другой патологии. По данным Dobson и Ikin, изогемагглютинины отсутствовали у 0,01 % здоровых лиц. Авторы связывали это с соматическими мутациями, приводящими к инактивации клонов В-клеток, запрограммированных на синтез соответствующих антител. Интересно, что родители, братья и сестры пробандов содержали изогемагглютинины, характерные для соответствующей группы крови. Возможно, синтез АВО-антител контролируется широко встречающимся доминантным геном и его редко встречающимся рецессивным молчащим аллелем. Лица без изогемагглютининов являются гомозиготными по указанному рецессивному аллелю.
В 1924 г. Bernstein предложил генетическую модель системы АВО. В соответствии с ней существуют 3 аллельных гена: О, А и В {в антропологии их обозначают как г, р и q соответственно). Ген А контролирует синтез антигена А, ген В - антигена В, ген О - молчащий - не кодирует синтеза какого-либо антигена, определяемого серологически. Лица группы 0(1) всегда гомозиготны по аллелю
О (генотип 0/0). Люди с группой AB(IV) гетерозиготны по генам А иВ (генотип А/В). Индивиды, имеющие группу А и В, могут быть гомо- (А/А и В/В) и гетерозиготными (А/О и В/О). Серологическими методами дифференцировать гомо- и гетерозиготность не удается. Тем не менее с определенной степенью вероятности можно сделать заключение о том, к какой из этих категорий относится данный индивид. Эритроциты гетерозигот содержат меньше антигенного материала, чем гомозиготы, что проявляется в меньшей агглютинабельности эритроцитов. Кроме того, эритроциты гетерозигот сильнее агглютинируются сыворотками анти-Н.
Групповую принадлежность членов семьи учитывают в судебной медицине при проведении экспертизы при спорном отцовстве или замене детей (Прокоп и Гёллер, А.К. Туманов и В.В. Томилин, А.К. Туманов [59], Yoshida). В частности у родителей АА х АА не может быть детей с группой крови В(Ш) или 0(1). Группа 0(1) исключена также, если один из родителей имеет группу крови AB(IV) (табл. 3.3).
Цис-АВ
В 1964 г. Seyfried и соавт. [194] описали польскую семью, в которой родители А2В х О имели детей А2В и О (рис. 3.1), что противоречило правилу наследования групп крови: дети в данной семье должны были иметь группу крови А или В. Полученные данные позволили предположить, что, как редкое исключение, гены А и В могут располагаться на одной хромосоме, в позиции цис, и передаваться в таком виде потомству.
При обследовании 1 млн японских доноров группа АВ выявлена у 112 710, из них 14 индивидов унаследовали цис-АВ. Подобный тип наследования группы крови был обнаружен у израильтян, корейцев и представителей других национальностей (Bennett и соавт. , Cho и соавт., Fukumori и соавт., Hummel и соавт. , Misfud и соавт., Pacuzska и соавт., Tzeng и соавт. , Yoshida и соавт. ).
Варианты наследования группы крови|
Фенотип родителей |
Генотип родителей |
Возможный фенотип (генотип) детей |
|
А* А |
АА хАА |
А (АА) |
|
АА *А |
А (АА или АО) |
|
|
АО *А |
А (АА или АО) или 0 (00) |
|
|
ВхВ |
ВВ*ВВ |
В (ВВ) |
|
ВВ*ВО |
В (ВВ или ВО) |
|
|
ВО х ВО |
В (ВВ или ВО) или 0 (00) |
|
|
АВ х АВ |
АВ х АВ |
А (АА) или В (ВВ) или АВ (АВ) |
|
ОхО |
00^00 |
0(00) |
|
Ах В |
АА хВВ |
АВ (АВ) |
|
АО х ВВ |
АВ (АВ) или В (ВО) |
|
|
АА х ВО |
АВ (АВ) или А (АО) |
|
|
АО х ВО |
АВ (АВ) или А (АО) или В (ВО) или 0 (00) |
|
|
АхО |
АА х 00 |
А (АО) |
|
АО х 00 |
А (АО) или 0 (00) |
|
|
\ “ А х АВ |
ААхАВ |
АВ (АВ) или А (АА) |
|
АО хАВ |
АВ (АВ) или А (АО) или В (ВО) |
|
|
ВхО |
ВВ х 00 |
В (ВО) |
|
ВО хОО |
В (ВО) или 0 (00) |
|
|
Цх АВ |
ВВ хАВ |
В (ВВ) или АВ (АВ) |
|
ВО хАВ |
АВ (АВ) или А (АО) или В (ВВ или ВО) |
|
|
АВ х 0 |
АВ х 00 |
А (АО) ши В (ВО) |
Серологические свойства эритроцитов цис-АВ несколько отличаются от обычных эритроцитов АВ (транс-АВ). Антиген А на них выражен слабее, однако его экспрессия выше, чем на эритроцитах А2В. Антиген В выражен слабо и представлен, как полагают Pacuzska и соавт., парциальной формой, напоминающей вариант В3 или Bw. В отдельных случаях экспрессия антигена В у лиц цис-АВ нормальная (Issitt и Anstee ).
в них антител анти-А и анти-В класса IgG (Д.В. Лабунов, И.В. Рау, М.А. Матвеева и др. , Н.Н. Меркулова и др. , В.А. Мороков и др., И.В. Рау, Judd ).
Более точно антитела АВО IgM и IgG, а также антитела, относящиеся к субклассам IgG,, IgG2, IgG3 и IgG4, определяют с помощью специально предназначенных для этого антиглобулиновых сывороток, дифференцирующих указанные антитела.
Установлено, что частота антител класса IgG увеличивается с возрастом. Так, по данным Е.А. Хромовой, у детей О, А и В в возрасте от одного года до 15 лет IgG-антитела анти-А, -В и -АВ выявляют в 45,5; 4,1 и 15,7 % случаев соответственно. Чаще всего IgG-антитела анти-А и анти-В выявляют у беременных. По данным Е.А. Хромовой , среди женщин группы О, А и В - в 76,2; 15,1 и 35,3 % случаев соответственно. Переключение синтеза антител с IgM на IgG инициируется повторными контактами с ксеногенными веществами, обладающими А- и В-подобной антигенной активностью. Как уже отмечено выше, у лиц с группой А и В в пуле синтезируемых анти-В- и анти-А-антител преобладают IgM, а у лиц с группой О - IgG. Активность групповых антител несколько выше у женщин, чем у мужчин. Выявлены сезонные колебания, в частности снижение активности указанных антител в осенний период (К.Н. Климова и др. ). Содержание IgM в сыворотке крови снижается в пожилом возрасте (Baumgarten и соавт. ).
Персистенция материнских эритроцитов в кровотоке новорожденного протекает соответственно закономерностям, наблюдаемым при трансплантации ал- логенных гемопоэтических клеток. Попадающие в кровоток ребенка в процессе родов гемопоэтические клетки матери (интернатальная миниалломиелотран- сплантация) могут создавать в его костном мозге временный очаг кроветворения. Выброс в кровоток ребенка иногруппных эритроцитов, продуцируемых переживающим материнским клоном, инициирует антителообразование у ребенка. Появившиеся антитела приводят к подавлению указанного клона. Полагаем, что это еще один материальный механизм возникновения антиэритроцитарных антител, ранее считавшихся спонтанными. В действительности эти антитела имеют хотя и необычное, но аллоиммунное происхождение.
Приводим случай обнаружения анти-С антител, который позволяет предположить именно такой механизм их происхождения (С.И. Донсков, И.С. Липатова).
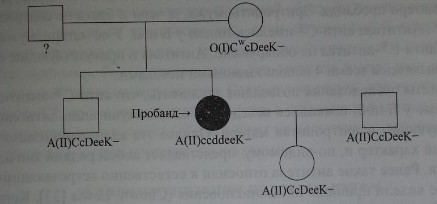
У родильницы Б-ной, 1977 г. рождения, в 2004 г. при плановом скрининге обнаружены анти-С антитела. В акушерском анамнезе Б-ной 5 беременностей от одного мужа: 1-я - в 1997 г., закончилась рождением ребенка с геморрагическим синдром, на третьи сутки ребенок умер; 2-я - в 1998 г., закончилась на раннем сроке выкидышем; 3-я - в 1999 г., закончилась медицинским абортом. 4-я - в 2000 г.,закончилась рождением здорового ребенка, 5-я - в 2004 г., закончилась медицинским абортом. Гемотрансфузий не было.
Выявление антител в сыворотках и фенотипирование эритроцитов проводили четырьмя методами: реакцией конглютинации в пробирках с 33 % полиглюкином и 10 % желатином, реакцией агглютинации на плоскости и в микроколонках с гелем. Идентификацию антител проводили желатиновым, гелевым и ферментным методами с использованием 11-клеточной панели стандартных эритроцитов.
Исследовали эритроциты и сыворотку (см. табл. 2,1) крови членов семьи Б-ной: мужа, дочери, матери и брата.
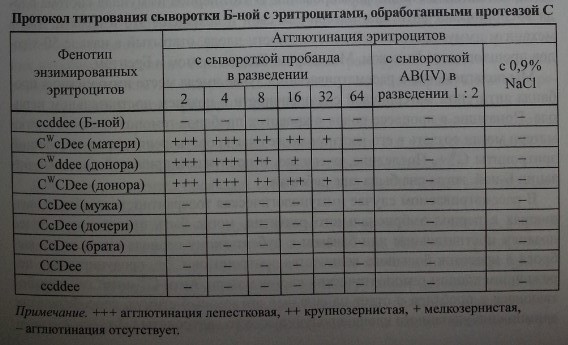
Сыворотка Б-ной реагировала в ферментном методе в разведении 1:16- Д 32 с 3 образцами С ^положительных эритроцитов, в том числе матери (табл. 2.2).
'' С собственными эритроцитами, эритроцитами мужа, брата и дочери, а также другими эритроцитами, не содержащими антигена С , сыворотка не реагировала, что еще раз подтверждало отсутствие антигена Cw в эритроцитах близких родственников.
Протокол титрования сыворотки Б-ной с эритроцитами, обработанными протеазой С
Примечание. +++ агглютинация лепестковая, ++ крупнозернистая, + мелкозернистая, агглютинация отсутствует.
В разновидности антител в дополнение к анти-А и анти-В (Н.М. Михайлова и др.). Антитела анти-А, содержатся одновременно с анти-А в сыворотках крови лиц группы В. Антитела анти-Н содержатся в сыворотках крови лиц, имеющих редкую группу крови Oh (тип Бомбей), но иногда встречаются в сыворотках крови лиц, имеющих группу крови А и АВ. Они относятся к Холодовым агглютининам, имеют низкий титр, при 37 °С не активны (Issitt и Anstee).
Новости медицины
Много миллионов человек в мире принимают статины, но исследования показывают, что только 55% из тех, кому рекомендуется принимать статины, принимают их. Это большая проблема, потому что исследования также показывают, что те из группы...
Связанное с беременностью высокое кровяное давление может привести к долгосрочным сердечным рискам, показывают новые исследования.
Кэролин Консия, столкнулась с более серьезными последствиями репрессий против назначения опиоидов, когда узнала, почему сын ее подруги покончил с собой в 2017 году.
Новое исследование показывает, что психические заболевания не являются фактором большинства массовых расстрелов или других видов массовых убийств.