Перед переливанием эритроцитов трансфузиолог по имеющимся документам устанавливает фенотип реципиента по 10 трансфузионно опасным антигенам эритроцитов и, если таковые отсутствуют, организует или выполняет самостоятельно фенотипирование реципиента. Далее трансфузиолог устанавливает, к какой из четырех условных категорий относится реципиент (рис. 36.1). Если в анамнезе реципиента нет указаний на имевшиеся беременности и переливания эритроцитов, его относят к категории 1. У реципиентов этой категории наименьший риск посттрансфузионных осложнений.
У реципиентов, относящихся к категории 2 и 3, риск постгрансфузионного осложнения возрастает. В этом случае необходимо предварительно исследовать кровь реципиента на наличие антиэритроцитарных антител. Это исследование должен выполнять специалист иммуносеролог в специализированной лаборатории. Подбор эритроцитов реципиентам, в крови которых обнаружены антитела (реципиентам категории 4), проводит только специалист иммуносеролог в лабораторных условиях.
Подбор доноров реципиентам всех указанных категорий осуществляют с учетом идентичности по 10 трансфузионно опасным антигенам эритроцитов, однако последнее обстоятельство не освобождает трансфузиолога от выполнения обязательных иммуносерологических исследований непосредственно перед трансфузией: определения группы крови у донора и реципиента, выполнения проб на индивидуальную совместимость и биологической пробы.
Соблюдение перечисленных правил гарантирует иммунологическую безопасность трансфузии эритроцитов.
К теории протективного действия иммуноглобулина антирезус
Механизм феномена отмены аллоиммунизации резус-отрицательных рожениц резус-антигеном плода посредством инъекции им анти-Э-антител после Первых родов до сих пор не имеет удовлетворительного объяснения. Считается, та пассивно введенные антитела связывают резус-положительные эритроциты ребенка, попавшие в кровоток матери в процессе родов, и далее инициируют их быструю элиминацию ретикулоэндотелиальной системой, тем самым предотвращая аллоиммунизацию. Однако также хорошо известно, что агглютинирующая способность и титр резус-антител не коррелируют с их способностью предупреждать аллоиммунизацию. Подавляющее большинство серий монокло-нальных антител, имеющих высокую авидность и огромный титр, протекторными свойствами не обладает.
Обращает на себя внимание тот факт, что при первичной иммунизации и ре-иммунизации титр антител варьирует в широких пределах. У одних людей он низкий, у других - чрезвычайно высокий.
В наших исследованиях (И.С. Липатова, СИ. Донсков [15]) при реиммуниза-ции сенсибилизированных лиц также отчетливо прослеживались колебания титра антител (табл. 36.2).
Таблица 36.2 Уровни антителообразования при реиммунизации антигеном D
|
Число инъекций |
Количество доноров |
Количество доноров, имевших уровень антител |
|||
|
низкий |
средний |
высокий |
сверхвысокий |
||
|
1 |
19 |
5 |
10 |
4 |
|
|
2 |
26 |
5 |
5 |
8 |
8 |
|
3 |
27 |
3 |
5 |
8 |
11 |
|
всего |
72 |
13(18%) |
20 (27,8 %) |
20 (27,8 %) |
19(26,4%) |
Изменения титра оценивали по количеству ступеней разведения сыворотки. Высоту иммунного ответа можно было условно разделить на 4 уровня:
сверхвысокий - повышение титра на 7 ступеней и более (1 : 512-1 : 8192); высокий - повышение титра на 5-6 ступеней (до 1 : 256); средний - повышение титра на 3-4 ступени (до 1 : 128); низкий - повышение титра на 1-2 ступени (до 1 : 32).
Неодинаковое повышение титра антител у аллоиммунизированных позволяет высказать предположение о существовании в организме человека специализированной индикаторной системы, контролирующей уровень (определяющей достаточность) антителообразования. Вырабатывающиеся антитела, по-видимому, содержат определенный сигнальный фрагмент, который приостанавливает их синтез (сигнализирует о его достаточности). У одних людей эти сигнальные фрагменты формируются в молекуле антител раньше (либо более активны), в результате чего синтез антител останавливается на относительно низком уровне, объем продукции антител небольшой, и последующая антигенная стимуляция не дает ожидаемого повышения титра. У других людей указанный сигнальный фрагмент формируется позднее, менее активен или вовсе не формируется. В этом случае антителообразование не ограничено, объем продукции
антдаея большой, и титр антител достигает высоких разведений. Не исключено, Щ именно этот механизм регуляции антителообразования лежит в основе предупреждения аллоиммунизации резус-отрицательных родильниц инъекцией им анти-О-антител.
Моноклональные антитела в отличие от поликлональных не обладают способностью предупреждать аллоиммунизацию резус-антигеном. Очевидно, МКА не содержат сигнальных фрагментов, отменяющих аллоиммунизацию. При получении МКА выбирают клоны, вырабатывающие высокоавид-ные антитела с высоким титром, наиболее пригодные для определения резус-антигена в серологических реакциях. Клоны, вырабатывающие антитела с низким титром, выбраковывают. Не исключено, что параллельно с антителами вырабатывается протеин с сигнальной вставкой - стоп-сигналом. Он не является антителом, но сопутствует антителам и является тем стоп-сигналом, который останавливает синтез антител. Этот протеин также выбраковывают. По-видимому, именно с этой выбраковкой связана неэффективность применения МКА анти-D в акушерской практике.
Можно с высокой степенью вероятности полагать, что способность антител реагировать invitroв серологических реакциях и способность препаратов, содержащих антитела, предотвращать аллоиммунизацию invivo- два разных свойства, присущих препаратам, содержащим антитела. Оба свойства не связаны друг с другом и не являются пропорциональными. Протекторное действие антител не усиливается параллельно увеличению их авидности и титра. Скорее, наоборот, антитела с высоким титром, в том числе МКА, в меньшей степени проявляют (или вовсе не проявляют) протективный эффект, в то время как поликлональные антитела, имеющие существенно более низкий титр, чем МКА, тормозят запуск иммунного ответа. Не исключено также, что антитела и протеин, несущий сигнальную вставку, - разные белки, одновременно присутствующие в поликлональном препарате. В моноклональных антителах протеин, несущий сигнальную вставку, отсутствует.
По-видимому, можно выделить два типа резус-антител: серологически высокоактивные, но не препятствующие запуску иммунного ответа на резус-антиген invivo, и серологически не столь активные, но отменяющие иммунный ответ invivo. Пока нет методических подходов, позволяющих с помощью серологических методов различить антитела, имеющие и не имеющие указанной выше сигнальной вставки - стоп-сигнала. Вместе с тем некоторые заделы в этом направлении имеются. В частности, обращает на себя внимание поведение нормальных лимфоцитов человека в реакции розеткообразования (рис. 36.2) с ал-логенными эритроцитами, нагруженными анти-Б-антителами (СИ. Донсков, Е.А. Зотиков [12]). Обработка эритроцитов одними образцами резус-антител приводила к розеткообразованию, в то время как обработка этих же эритро-ЩШъ другими образцами резус-антител, не отличавшимися по активности, не инициировала розеткообразования.
Розеткообразование ингибировалось сыворотками против имму-рйяюбулинов человека, что свидетельствовало о зависимости этой реакции от иммуноглобулиновых рецепторов, имеющихся на поверхности В-клеток и способных, как известно, реагировать с Fc-фрагментом 78-иммуноглобулинов, а также комплексом антиген - антитело.
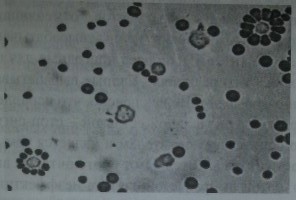
Два типа розеткообразующих клеток человека.
Вверху справа — лимфоцит, образовавший розетку с эритроцитами, сенсибилизированными неполными резус-антителами (В-лимфоцит), внизу слева - лимфоцит, образовавший розетку с эритроцитами барана (Т-лимфоцит).
Следует еще раз подчеркнуть, что не все сыворотки, содержащие неполные резус-антитела, способны инициировать аллогенное розеткообразование. По этому свойству они могут быть разделены на две группы: розеткообразую-щие ирозетконеобразующие.
Способность резус-антител вызывать прилипание лимфоцитов не была связана с принадлежностью сыворотки к какой-либо из групп системы АВО, не зависела от антигенов Gma и Gmb, а также от пола и возраста лиц, от которых были получены антитела. Розеткообразование усиливалось, если эритроциты нагружали несколькими антителами.
Не установлено, как соотносится розеткообразующая способность антител с их протекторным действием и нельзя ли по розеткообразующим свойствам aHTH-D-антител детектировать их способность отменять аллоиммму-низацию?







