Поиск по сайту
Наш блог
Это странная ситуация: вы соблюдали все меры предосторожности COVID-19 (вы почти все время дома), но, тем не менее, вы каким-то образом простудились. Вы можете задаться...
Как диетолог, я вижу, что многие причудливые диеты приходят в нашу жизнь и быстро исчезают из нее. Многие из них это скорее наказание, чем способ питаться правильно и влиять на...
Овес-это натуральное цельное зерно, богатое своего рода растворимой клетчаткой, которая может помочь вывести “плохой” низкий уровень холестерина ЛПНП из вашего организма....
Если вы принимаете витаминные и минеральные добавки в надежде укрепить свое здоровье, вы можете задаться вопросом: “Есть ли лучшее время дня для приема витаминов?”
Ты хочешь жить долго и счастливо. Возможно, ты мечтал об этом с детства. Хотя никакие реальные отношения не могут сравниться со сказочными фильмами, многие люди наслаждаются...
Приседания и выпады-типичные упражнения для укрепления мышц нижней части тела. Хотя они чрезвычайно распространены, они не могут быть безопасным вариантом для всех. Некоторые...

Ученые из Стэнфордского университета разработали программу предсказывающую смерть человека с высокой точностью.

Глава Минздрава РФ Вероника Скворцова опровергла сообщение о падении доходов медицинских работников в ближайшие годы. Она заявила об этом на встрече с журналистами ведущих...

Федеральная служба по надзору в сфере здравоохранения озвучила тревожную статистику. Она касаются увеличения риска острой кардиотоксичности и роста сопутствующих осложнений от...

Соответствующий законопроект внесен в палату на рассмотрение. Суть его заключается в нахождении одного из родителей в больничной палате бесплатно, в течении всего срока лечения...
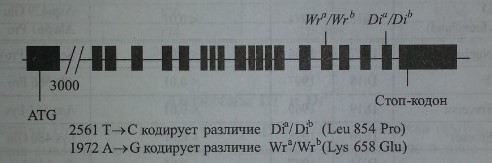
В настоящее время в групповую эритроцитарную систему Diego (Диего) включен 21 антиген (табл. 12.1), из них два редких (Dia и Wra) являются антитетичными по отношению к двум частым антигенам (Dib и Wrb) соответственно. Остальные 17 антигенов не имеют антитетичных партнеров и встречаются крайне редко у представителей всех обследованных популяций и этнических групп. Антиген Dia представляет определенный интерес для антропологов как своеобразный расовый маркер, поскольку встречается исключительно у монголоидов. К настоящему времени установлено, что специфичность антигенов Diaи Dib обусловлена заменой пролина на лейцин в позиции 854 на протеине полосы 3, встроенном в мембрану эритроцитов. Эта структура, выполняющая функцию транспортера анионов в клетке, также обозначается как АЕ1 или CD233.
Генная карта локуса DI (SLC4A 1, АЕ1, ЕРВЗ).
Классификация антигенов системы Diego
|
Обозначение |
Год открытия |
Частота, % |
Молекулярная основа |
|
|
авторское |
ISBT |
|||
|
Dia (Diego) |
Dil |
1955 |
< 0,01; 5-12 - монголоиды, 36 - индейцы Южной Америки |
Leu 854 Pro |
|
Dib (Luebano) |
Di2 |
1967 |
> 99,9; 90 - монголоиды, 64 - индейцы Южной Америки |
Pro 854 |
|
Wra (Wright) |
Di3 |
1953 |
< 0,01 |
Lys 658 Glu |
|
Обозначение авторское |
ISBT |
открытия |
Частота, % |
Молекулярная основа |
|
Wrb (Fritz) |
Di4 |
1971 |
>99,9 |
Glu 658 |
|
Wda (Waldner) |
Di5 |
1983 |
<0,01 I |
Met 557 Val |
|
Rba (Redelberger) |
Di6 |
1978 |
< 0,01 |
Leu 548 Pro |
|
WARR (Warrior) |
|
1991 |
< 0,01 |
He 552 Thr |
|
ELO |
|
1979 |
<0,01 |
Trp 432 Arg 0») |
|
Wu (Wulfsberg) |
|
1967 |
< 0,01 |
Ala 556 Gly '' |
|
Bpa (Bishop) ^ |
DilO |
1964 |
< 0,01 |
Lys 569 Asn |
|
Moa (Moen) |
Dill |
1972 |
<0,01 |
His 656 Arg |
|
Hga (Hughes) |
Dil2 |
1983 |
< 0,01 |
Cys 656 Arg |
|
Vga, Van, Vugt |
Dil3 |
1981 |
< 0,01 |
His 555 Tyr |
|
Swa (Swann) |
Dil4 |
1959 |
<0,01 |
Gin (Trp) 646 Arg |
|
BOW (Bowyer) |
Dil5 |
1988 |
< 0,01 |
Ser 561 Pro |
|
NFLD (Newfoundland) |
Dil6 |
1984 |
<0,01 |
Asp 429 Glu Ala 561 Pro |
|
Jna (Nunhart) |
Dil7 |
1964 |
<0,01 |
Ser 566 (Pro) |
|
KREP |
Dil8 |
1997 |
< 0,01 |
Ala 566 Pro |
|
Tra, Traversu |
Dil9 |
1960 |
< 0,01 |
Asn 551 Lys |
|
Fra (Froese) |
Di20 |
1978 |
< 0,01 |
Lys 480 Glu |
|
SW1 |
Di21 |
1987 |
<0,01 |
Trp 646 Arg |
Различия другой пары антигенов (Wra и Wrb) обусловлены аминокислотной заменой Lys 658 Glu в белке полосы 3. Эритроциты с дефицитом гликофорина А имеют группу Wr(a-b-). Таким образом, для экспрессии на эритроцитах антигена Wrb (DI4) требуется присутствие как белка полосы 3, так и гликофорина А. Остальные антигены системы Diego являются результатом точковых мутаций в различных участках гена DI9приводящих к аминокислотным заменам в соответствующих участках протеина полосы 3 (рис. 12.1). Новые аминокислотные последовательности иммуногенны и способны стимулировать синтез антител, специфически их распознающих. Нулевой фенотип, Di(a-b-), в системе Diego не известен. Ген SLC4A1, контролирующий синтез белка полосы 3, картирован на хромосоме 17 в позиции 17ql2-q21. Структура гена исследована (табл. 12.2).
Организация гена SLC4A1
|
Экзон |
Количество пар оснований |
Позиция кодируемых аминокислот |
Размер интрона, кб |
|
1 |
582 |
|
>3 |
|
2 |
83 |
1-5 |
0,125 |
|
3 |
91 |
6-36 |
0,998 |
|
4 |
62 |
37-57 |
0,757 |
|
5 |
181 |
57-117 |
0,095 |
|
6 |
136 |
117-162 |
0,472 |
|
7 |
124 |
162-203 |
0,227 |
|
8 |
85 |
204-232 |
0,152 |
|
9 |
182 |
232-292 |
0,539 |
|
10 |
211 |
293-363 |
0,232 |
|
11 |
195 |
363-428 |
0,178 |
|
12 |
149 |
428^477 |
0,114 |
|
13 |
195 |
478-542 |
1,503 |
|
14 |
174 |
543-600 |
0,377 |
|
15 |
90 |
601-630 |
0,543 |
|
16 |
167 |
631-686 |
1,126 |
|
17 |
254 |
686-771 |
1,527 |
|
18 |
170 |
771-827 |
0,086 |
|
19 |
174 |
828-885 |
0,620 |
|
20 |
2146 |
886-911 |
|
Антиген Dia описан Layrisse и соавт. [95] в 1955 г. Антитела против этого антигена вызвали гемолитическое заболевание у новорожденного мисс Diego, в семье европейцев и потомков коренных индейцев (Каракас, Венесуэла). Антитела, идентифицирующие антиген Dib, антитетичный фактору Dia, описаны 12 годами позднее Thompson и соавт. [164].
Антиген Dia не является редким среди индейцев Южной Америки (табл. 12.3). У них его выявляли с частотой 36 % (Allen, Corcoran [6]), у некоторых племен частота антигена Dia достигала 60-70 % [95, 99]. У представителей других монголоидных рас фактор Dia встречался с частотой 5-12 %.
Этот фактор найден и среди индейцев Северной Америки, хотя на этом континенте его частота оказалась ниже. Интересен тот факт, что антиген Dia встречается реже среди аборигенов Аляски и Канады, чем Сибири. Среди народов Юго-Восточной Азии антиген Dia выявляли с частотой 2-12 %, среди японцев частота Dia оказалась выше (12 %), чем у китайцев (5 %) (Lewis и соавт. [100], Layrisse, Arends [93]).
При проведении популяционных исследований в СССР Х.Р. Неванлинна [1] среди 500 обследованных эстонцев нашел 2 с фенотипом Di(a+). У 1 из 105 обследованных коми, жителей села Визинги, также был выявлен антиген Dia(Eriksson, Frants [43]). Однако следует заметить, что в этом селе ранее проживало несколько китайских семей. Таким образом, не исключен импорт гена Dia в популяцию коми из китайской диаспоры.
Таблица 12.3
Распределение антигена Dia у разных народов
|
Популяция |
Число обследованных |
Частота Dia |
Источник |
|
|
абс. число |
% |
|||
|
Индейцы Chippewa (США) |
148 |
16 |
10,81 |
[100] |
|
Индейцы Penobscot (США) |
249 |
20 |
8,03 |
[6] |
|
Мексиканцы (США) |
1685 |
172 |
10,21 |
[42] |
|
Индейцы Kainganges (Бразилия) |
48 |
26 |
54,16 |
[99] |
|
Индейцы Mayan (Гватемала) |
255 |
57 |
22,35 |
[23] |
|
Индейцы Carib (Венесуэла) |
121 |
43 |
35,54 |
[99] |
|
Индейцы Arawaco (Венесуэла) |
152 |
8 |
5,26 |
[99] |
|
Коряки (Аляска, США, Канада) |
1477 |
2 |
0,14 |
[122] |
|
Коряки (Сибирь) |
86 |
18 |
20,93 |
[122,165] |
|
Японцы |
2427 |
244 |
10,05 |
[118] |
|
Китайцы |
617 |
32 |
5,19 |
[122] |
|
Китайцы (Тайвань) |
1000 |
32 |
3,20 |
[109] |
|
Корейцы |
277 |
17 |
6,14 |
[174] |
|
Индусы (Северная Индия) |
377 |
15 |
4,00 |
[122] |
|
Поляки |
9661 |
45 |
0,47 |
[89] |
|
Американские негры |
827 |
1 |
0,12 |
[122] |
|
Европейцы |
4462 |
1 |
0,02 |
[42,92,99,143] |
|
Белые американцы |
1000 |
[99] |
||
|
Негры Ганы |
107 |
[94] |
||
|
Австралийские аборигены |
1374 |
[152] |
||
|
Папуасы (Папуа - Новая Гвинея) |
1741 |
[152] |
||
У лиц белой расы этот антиген практически не встречается (Layrisse и соавт. [95, 94, 99], Lin-Chu и соавт. [109], Simmons и соавт. [153], Graninger [51], Won и соавт. [174]).
Случаи выявления лиц Di(a+) среди поляков и австрийцев объясняли дрейфом гена Dia в период монголо-татарского нашествия в Западную Европу в XIII-XIV веках (Kusnierz-Alejska, Bochenek [89]). Известен один индивид белой расы, гомозиготный по гену Dia и проживавший в Австрии (Issitt, Anstee [65]).
Антиген Dia отсутствует у австралийских аборигенов, жителей островов Тихого Океана и крайне редко встречается у негроидов.
Issitt и Anstee [65] призывают критически относиться к сообщениям о частоте фенотипа Di(a+) среди различных популяций в силу ряда причин.
Во-первых, по их мнению, величина выборок, варьирующая от 29 до 5259 обследованных, не является репрезентативной.
Во-вторых, при обследовании одних и тех же этнических групп получены противоречивые результаты. Так, в одном из исследований среди 1 тыс. китайцев Тайваня фенотип Di(a+) был найден в 32 случаях, тогда как в другом среди 772 обследованных он не был выявлен ни разу. Причины таких расхождений, как полагают Issitt и Anstee, трудно объяснить. Противоречие может быть обусловлено тем, что для исследования была использована сыворотка, которая, помимо антител aHTH-Dia, могла содержать антитела к одному из редких антигенов системы MN (Mta, Mur, MUT, Hil, MINY), встречающихся у китайцев.
В-третьих, разные исследователи сообщали о выявлении антигена Dia с частотой от 1 : 4462 среди европейцев до 1 :827 среди американских негров. Фенотип Di(a+) не найден среди 1741 жителя Папуа - Новой Гвинеи, 1374 австралийских аборигенов, 1 тыс. американских негров и 107 жителей Ганы (Африка). В то же время есть сообщения о высокой частоте фенотипа Di(a+) в тех же этнических группах. Большинство из таких исследований было проведено с использованием антител анти-Di3, явившихся причиной ГБН или появившихся у реципиентов, получавших трансфузии крови. В этих случаях антиген Dia был выявлен среди англичан, ирландцев а также среди белых американцев (Issitt и Anstee [65]). Сведения о возможности смешения с монголоидами отсутствовали. Одна жительница Германии, венгерка по национальности, имела фенотип Di(a+b-), т. е. правомерно полагать, что она гомозиготна по гену Dia. Вместе с тем Issitt и Anstee [65] отмечают, что факты обнаружения антигена Dia в отдельных английских и ирландских семьях вряд ли связаны с завоеваниями монголов.
Как уже отмечалось выше, обнаружение фенотипа Di(a+) среди поляков объясняли заносом гена Dia в эту этническую группу во времена монголо-татарского нашествия. Наибольшая частота фенотипа Di(a+) (0,66 %) выявлена на Юго-Востоке Польши (область вторжения монголо-татар), а в западных районах этой страны частота антигена Dia составила 0,3 %. Оригинальная публикация содержит карту Польши, на которой отражены вариации частоты антигена Dia и районов, где имела место монголо-татарская экспансия.
Если гипотеза относительно генного дрейфа верна, то среди населения определенных регионов России и Украины антиген Dia также должен встречаться с частотой, близкой к таковой среди поляков. Можно полагать, что этот антиген имеется у татар, башкир, марийцев, мордвы, калмыков. Однако распределение антигена Dia среди жителей России пока не изучено.
Й&аздо меньше популяционных исследований было проведено с использованием сывороток aHTH-Dib (Mourant и соавт. [122], Tills и соавт. [165], Edwards-Moulds, Alperin [42], Issitt и соавт. [70]). При этом было установлено, что все без исключения 01ь-отрицательные индивиды имели группу Di(a+). Нулевой фенотип в системе Diego [Di(a-b-)] найден не был.
Антигены Dia и Dib полностью развиты на эритроцитах новорожденных к моменту рождения (Thompson и соавт. [164], Edwards-Moulds, Aiperin [42], Layrisse, Arends [92], Lewis и соавт. [104], Tatarsky и соавт. [162], Feller и соавт. [44], Nakajima и соавт. [124]).
Антигены Wra и Wrb (Wright и Fritz)
Антигены Wra и Wrb на протяжении многих лет после их обнаружения не удавалось отнести к какой-либо из известных эритроцитарных групповых систем. Учитывая антитетичность связи, их в 1991 г. выделили в коллекцию 211 WRIGHT, где они были обозначены WR1 (211.001) и WR2 (211.002). Лишь в 1995 г. была показана принадлежность этих антигенов к системе Diego, куда они были внесены с новыми обозначениями - Di3 и Di4.
Редко встречающийся антиген Wra (Wright), описанный Holman [59] в 1953 г., имеет частоту менее 1 :1000 среди европеоидов (табл. 12.4). Обширные исследования частоты антигена Wra были проведены среди представителей разных этнических групп. Он был обнаружен среди монголоидов и некоторых негроидов, но не был найден среди австралийских аборигенов, жителей Папуа -Новой Гвинеи (Simmons [152]).
Исследования во многих семьях показали аутосомное доминантное наследование гена Wra в соответствии с законом Менделя (Holman [59], Kornstad [83], Metaxas, Metaxas-Buhler [117], Lewis и соавт. [103, 107]). Результаты иследования в одной семье указывали на возможность сцепления генов, контролирующих экспрессию антигенов Wra и Sda (Lewis и соавт. [103]).
Таблица 12.4
Частота антигена Wra у европеоидов
|
Популяция |
Количество обследованных |
Выявлено Wr(a+) |
Частота Wra, % |
Источник |
|
Англичане |
45 631 |
36 |
0,0008 |
[28] |
|
Англичане |
5 253 |
2 |
0,0014 |
[171] |
|
Шотландцы |
1000 |
1 |
0,0010 |
[137] |
|
Норвежцы |
5 138 |
[83] |
||
|
Норвежцы |
3 140 |
2 |
0,0006 |
[83] |
|
Швейцарцы |
3 753 |
2 |
0,0005 |
[117] |
|
Итальянцы |
6 350 |
7 |
0,0011 |
[ПО] |
|
Чехи |
1 500 |
1 |
0,0007 |
[88] |
|
Американцы (Бостон) |
2 784 |
3 |
0,00011 |
[170] |
|
Американцы (Нью Йорк) |
5 000 |
5 |
0,0010 |
[52] |
|
Американцы (Огайо) Аборигены Австралии Аборигены Папуа - Новая Гвинея |
7 000 |
ООО |
ООО |
[113] [152] [152] |
Антиген Wra полностью развит на эритроцитах к моменту рождения, однако его выраженность варьирует.
Символ анти-\¥гь было впервые использован Adams и соавт. [4] для обозначения антител, найденных в сыворотке крови женщины по фамилии Fritz, и открывавших часто встречающийся антиген, антитетичный Wra. Эритроциты сенсибилизированной женщины сильно реагировали с антителами affra-Wra, поэтому имелись основания полагать, что они несут двойную дозу указанного антигена. Антитела сыворотки ее крови проявляли эффект дозы, реагируя более интенсивно с эритроцитами Wr(a-), чем с эритроцитами Wr(a+). Эритроциты второго пробанда Wr(a+b-), содержащего антитела анти-\¥гь, несколько отличались от эритроцитов мисс Fritz, поскольку слабо реагировали с моноклональными антителами анти-Wr15 (Dahr et al [34]). Эффект дозы антител анти-АУга и
aHTH-Wrb с эритроцитами Wr(a+b~), Wr(a+b+) и Wr(a-b+) позднее был подтвержден с помощью иммуноферментного варианта антиглобулинового теста (Wren, Issitt [175]).
Секвенирование кДНК протеина полосы 3 вдавило замену кодонов G 1972 А в экзоне 16. Последняя обусловливает замену глютаминовой кислоты на лизин в положении 58 на четвертой экстрацеллюлярной петле белка полосы 3 (Bruce и соавт. [17]). У 3 индивидов, гомозигот Wr(a-b+), имелся кодон для Glu 58, а у гетерозигот Wr(a+b+) - кодоны как для Glu 58, так и Lys 58.
Антигены Wra и Wrb устойчивы к действию протеолитических ферментов (трипсин, химотрипсин, папаин, фицин, бромелин, проназа), донаторов суль-фгидрила и АЕТ (Daniels [36], Ring и соавт. [146]).
Указанные антигены не были выявлены на лимфоцитах, моноцитах и гранулоцитах в периферической крови.
Антитела анти-Di* и анти-В1ь
Анти-Di*
Первые 3 образца антител airra-Dia были найдены у женщин, дети которых страдали тяжелой формой ГБН, а новорожденный мисс Diego погиб от указанного заболевания (Levine и соавт. [98,99], Tatarsky и соавт. [162]). В последующие годы были найдены другие образцы антител ajfra-Dia, последние часто вырабатывались во время беременности, многие из них явились причиной ГБН (Riches и соавт. [143], Kusnierz-Alejska, Bochenek и соавт. [89], Graninger [51], Alves De Lima, Berthier [7], Zupanska и соавт. [185]). В одном случае антитела anra-Di3, выявленные у австралийской женщины белой расы, имели естественное происхождение (Simmons и соавт. [153]).
Антитела анти-Di3 способны вызывать посттрансфузионные реакции немедленного типа (Hinckley, Huestis [58]), однако в публикации указанных авторов сообщается об одновременном присутствии в сыворотке крови больного антител анти-с, поэтому осталось невыясненным, какие именно (анти-с или анти-Dia) из них послужили причиной гемотрансфузионного осложнения.
Thompson и соавт. [164], Yasuda и соавт. [177] описали замедленные гемолитические посттрансфузионные реакции, обусловленные антителами анти-ОК
Панели стандартных эритроцитов, используемые для рутинного скрининга иррегулярных антиэритроцитарных антител, обычно не содержат клеток Di(a+), поэтому антитела aHra-Dia, как правило, не выявляют при таких исследованиях.
В странах Америки опасность посттрансфузионных реакций, обусловленных антителами aHTH-Dia, выше, чем в Европе, поскольку частота доноров Di(a+) там существенно выше. Бразильскими авторами (Zago-Novaretti и соавт. [181]), изучавшими специфичность антител среди реципиентов, получавших множественные трансфузии, антитела анти-Di3 были найдены у 4 из 112 (3,6 %).
Airra-Dib
Имеются сообщения о ГБН, вызванной анти-01ь-антителами. Для лечения новорожденных потребовались обменные переливания крови (Ishimori и соавт. [64], Orlina и соавт. [129], Uchikawa и соавт. [166]).
Описан случай, когда антитела airra-Dib клинических проявлений ГБН не вызвали, несмотря на положительный прямой антиглобулиновый тест с эритроцитами
новорожденного и принадлежность антител к субклассу IgG3 (Habash и соавт. [54]). В тестах с монослоем моноцитов антитела aHin-Dib вызывали более высокий уровень адгезии и фагоцитоза с клетками Di(a-b+), чем Di(a+b+) (Lin и соавт. [108]). Антитела airra-Dib естественного происхождения не описаны. У 2 из 74 больных аутоиммунной гемолитической анемией найдены аутоантитела aHra-Dib, присутствовавшие наряду с антителами других специфичностей (Daniels [37]). В одном случае аутоантитела airra-Dib вызвали аутоиммунную гемолитическую анемию с выраженными клиническими проявлениями (Issitt и соавт. [66]).
Аллоиммунные антитела анти-Di3 и анти-Di15 чаще присутствуют в виде моноспецифических, реже их выявляли в сыворотках одновременно с антителами другой специфичности. Указанные антитела чаще представлены субклассами IgGl и IgG3 (Riches и соавт. [143], Kusnierz-Alejska, Bochenek [89], Alves De Lima, Berthier [7], Zupanska и соавт. [185], Habash и соавт. [54]). Некоторые образцы антител связывали комплемент и вызывали гемолиз эритроцитов in vitro (Kusnierz-Alejska, Bochenek [89], Mollison и соавт. [119]). Описаны агглютинины с указанной специфичностью (Simmons и соавт. [153]). Оптимальным методом выявления антител анти-Б1а и aHTH-Dib является антиглобулиновый.
Японские исследователи (Miyazaki и соавт. [118]) сообщили о 2 гете-рогибридомах aHTH-Dia, полученных слиянием клеток мышиных миелом с В-лимфоцитами лиц, сенсибилизированных к указанному антигену. Одна из гибридом продуцировала антитела IgM, взаимодействующие в прямой реакции агглютинации в солевой среде, другая секретировала антитела IgG, которые реагировали в непрямой антиглобулиновой пробе.
Антитела анти-Wr3 встречаются часто. В различных сообщениях их частота среди здоровых лиц варьирует от 1: 13 (McGuire, Funkhouser [113]) до 1 : 56-1 : 100 (Wallis и соавт. [171], Greendyke, Banzhaf [52], Lubenko, Contreras [111], Hardman, Beck [55]). Частота указанных антител существенно выше среди больных, родильниц и сенсибилизированных лиц, имеющих аллоантитела другой специфичности (Wallis и соавт. [171]).
Greendyke, Banzhaf [52] обнаружили анти^га-антитела у каждого 3-го больного аутоиммунной гемолитической анемией.
С.А. Фатьянов и соавт. [2, 3] исследовали 1823 сыворотки крови здоровых лиц (доноров крови), беременных, сенсибилизированных к антигенам системы Rh, а также пациентов с сосудистой патологией (атеросклероз сосудов нижних конечностей, варикозное расширение вен, тромбофлебит) и заболеваниями соединительной ткани (ревматоидный артрит, системная красная волчанка) на наличие антител к антигену Wra. Антитела выявляли непрямым ан-тиглобулиновым и ферментным методами с эритроцитами редких фенотипов: OCCDeeWr(a+), OccDEeWr(a+) и OccddeeWr(a+) - предоставленными доктором Marcela Contreras и доктором Jeoff Poole из Национальной службы крови Великобритании (Лондон, Бристоль). Антитела анти-Wr3 выявили у 1,2 % доноров, у 10,51 % беременных, у 11,42% больных системными заболеваниями соединительной ткани, у 17,83 % больных сосудистой патологией. Среди Rh-отрицательных лиц, аллоиммунизированных антигеном D, частота этих антител составила 18,52 %.
По мнению некоторых авторов, образование антител aHTH-Wra в организме Wra-OTpn4a^bHbix лиц в отсутствие специфической стимуляции может указывать на существование особого иммунного механизма элиминации эритроцитов in vivo, в основе которого лежит модификация протеина полосы 3 в мембране эритроцитов с возникновением de novo Wra-noflo6Hbix антигенных детерминант. В частности, присутствие анти^га-антител коррелировало с интенсивностью гемолиза эритроцитов in vivo (Issitt, Anstee [65]).
Первые 2 найденных образца антител aHra-Wra явились причиной тяжелой ГБН. Позднее появились другие аналогичные сообщения (Holman [59], Arriaga и соавт. [9], Wiener, Brancato [173], Daw [41], Jorgensen, Jakobsen [77]). Антитела анти-Wr3 описаны также в качестве причины гемолитически ансфузионных реакций (Metaxas, Metaxas-Buhler [117], van Loghem и соавт. [168]).
Несмотря на высокую частоту антител aHTH-Wra, случаи ГБН, так же как и посттрансфузионные реакции, обусловленные ими, регистрируют редко (Lubenko, Contreras [111]).
Как уже отмечено выше, анти-\Уга-антитела часто присутствуют одновременно с аллоантителами другой специфичности. Это создает дополнительные трудности при производстве серологических стандартов из аллогенных сывороток, поскольку антитела aHTH-Wra требуется адсорбировать, для чего необходимы эритроциты редкого фенотипа Wr(a+) (Byrne, Byrne [22]).
К настоящему времени получены мышиные моноклональные антитела анти-Wra класса IgG (гибридома BGU1-WR). Для получения гибридомы животных иммунизировали эритроцитами человека Wr(a+) (Ring и соавт. [146]).