Поиск по сайту
Наш блог
Это странная ситуация: вы соблюдали все меры предосторожности COVID-19 (вы почти все время дома), но, тем не менее, вы каким-то образом простудились. Вы можете задаться...
Как диетолог, я вижу, что многие причудливые диеты приходят в нашу жизнь и быстро исчезают из нее. Многие из них это скорее наказание, чем способ питаться правильно и влиять на...
Овес-это натуральное цельное зерно, богатое своего рода растворимой клетчаткой, которая может помочь вывести “плохой” низкий уровень холестерина ЛПНП из вашего организма....
Если вы принимаете витаминные и минеральные добавки в надежде укрепить свое здоровье, вы можете задаться вопросом: “Есть ли лучшее время дня для приема витаминов?”
Ты хочешь жить долго и счастливо. Возможно, ты мечтал об этом с детства. Хотя никакие реальные отношения не могут сравниться со сказочными фильмами, многие люди наслаждаются...
Приседания и выпады-типичные упражнения для укрепления мышц нижней части тела. Хотя они чрезвычайно распространены, они не могут быть безопасным вариантом для всех. Некоторые...

Ученые из Стэнфордского университета разработали программу предсказывающую смерть человека с высокой точностью.

Глава Минздрава РФ Вероника Скворцова опровергла сообщение о падении доходов медицинских работников в ближайшие годы. Она заявила об этом на встрече с журналистами ведущих...

Федеральная служба по надзору в сфере здравоохранения озвучила тревожную статистику. Она касаются увеличения риска острой кардиотоксичности и роста сопутствующих осложнений от...

Соответствующий законопроект внесен в палату на рассмотрение. Суть его заключается в нахождении одного из родителей в больничной палате бесплатно, в течении всего срока лечения...
- Категория: Система Scianna и система Dombrock
К системе Scianna (Сцианна) отнесены семь антигенов (табл. 15.1). Два из них - Scl и Sc2 - антитетичные, один - редко встречающийся Sc4 (Radin) и четыре часто встречающихся антигена: Sc3, Sc5 (STAR), Sc6 (SCER) и Sc7 (SCAN). Антиген Sc3 отсутствует только у лиц с нулевым фенотипом - Scnull
К моменту рождения антигены Scianna хорошо развиты (Rausen и соавт. [32])
Антигены системы Scianna
|
Обозначение |
Год |
Частота, % |
|||
|
авторское |
традиционное |
ISBT |
открытия |
включения в систему |
|
|
Sm, Scianna |
Scl |
SCI |
1962 |
1974 |
>99,9 |
|
Bua, Bullee |
El!Sc2 |
W SC2 I |
1962 |
1974 |
0,3 |
|
Отсутствует |
Sc3 |
SC3 |
1980 |
1980 |
>99,9 |
|
Rd, Rda, Radin |
Sc4 |
SC4 |
1967 |
2003 |
0,01-0,5 |
|
STARfe- |
Sc5 |
SC5 |
1980 jj |
2005 |
>99,9 Щ |
|
SCER |
Sc6 |
SC6 |
U 1980 j |
2005 |
Щ >99,9 |
|
SCAN |
Sc7 |
SC7 ^ |
1980 |
2005 |
>99,9 Ш |
История открытия
В 1962 г. Schmidt и соавт. [33] нашли антитела к антигену Sm, который не удалось отнести к какой-либо из известных групповых систем. Годом позже Anderson и соавт. [1] открыли редкий антиген Bua (Bullee), который также невозможно было причислить к какой-либо системе. В 1963 г. Lewis и соавт. [16] сообщили о результатах обследования семьи, в которой Schmidt и соавт. впервые выявили лиц Sm+ и Sm-. Эритроциты Sm- давали сильную агглютинацию с сывороткой анти-Виа. Эритроциты Sm+ реагировали с сывороткой анти-Виа слабее. Полученные данные позволили авторам предположить, что эритроциты Sm - несут двойную дозу антигена Виа и что антигены Sm и Виа могут быть связаны антитетичными отношениями. В 1967 г. эти же авторы получили данные, подтверждавшие антитетичную связь антигенов Sm и Bua (Lewis и соавт. [15]). Они обследовали 21 ребенка от родительских пар Sm-Bu(a+) х Sm+Bu(a) и Sm+Bu(a+) х Sm+Bu(a+). Трое детей были Sm-Bu(a+), 7 имели фенотип Sm+Bu(a-). Среди детей не было ни одного Sm-Bu(a-).
Отсутствие нулевого фенотипа, а также тот факт, что все обследованные имели антиген Виа, Sm или оба одновременно, указывают на аллельность генов Виа и Sm и, соответственно, на антитетичность детерминируемых ими антигенов.
В 1974 г. Lewis и соавт. [19] получили данные, свидетельствовшие о независимости генов SmnBua от других генных локусов, контролирующих групповые аллоантигены. Новая антигенная система получила наименование «Scianna» по фамилии семьи, в которой были выявлены антитела анти-Sm, а также индивиды Sm+ и Sm-. Антигены Sm и Виа получили обозначение Scl и Sc2, контролирующие их гены были обозначены как Sc1 nSc2 (Lewis, Kaita [18]).
В 1973 г. McCreary и соавт. [22] сообщили о результатах серологического обследования жителей одного из атоллов Маршалловых островов в южной части Тихого океана (Микронезия). Среди этой группы населения были распространены браки между кровными родственниками. Обследование было начато в связи с обнаружением индивида Sc:-l,-2. В сыворотке его крови присутствовали антитела с высокой частотой реагирования. Позднее были выявлены лица с таким же фенотипом и наличием антител аналогичной специфичности (Nason и соавт. [26]). Антитела получили обозначение aHTH-Sc3. Установлено, что аллель Sc1 кодирует появление антигенов Scl и Sc3, Sc2- Sc2 и Sc3. Стало очевидным, что в указанной системе встречается молчащий аллель Sc и, соответственно, гомозиготы Sc/Sc имеют фенотип Sc:-1,-2,-3.
Антигены Scl и Sc2
Частота встречаемости антигена Scl исключительно высока. При обследовании 269 ООО доноров в Лондоне выявлен только один с фенотипом Sc:-1 (Кауе и соавт. [14]). Эта редкая группа не установлена ни у одного из 1600 белых американцев (Schmidt и соавт. [33], Lewis и соавт. [19]) и 29 737 валлийцев, проживающих на полуострове Уэлс (Великобритания) (Gale и соавт. [11]).
Антиген Sc2, наоборот, встречается редко (табл. 15.2). Среди канадцев частота антигена Sc2 варьировала от 0 до 1,7 %. Из 1000 канадцев 983 были Sc:l,-2; 17 - Sc:l,2; фенотип Sc:—1,2 не найден. Среди жителей Европы антиген Sc2 распределялся более равномерно (см. табл. 15.2).
Расчеты показали, что ген Sc1 имеет частоту 0,9915, Sc2 - 0,0085, а генотипы Sc'Sc7, Sc'Sc2 и Sc2Sc2 встречаются с частотой 0,9831, 0,0168 и 0,0001 соответственно.
Антиген Scl полностью развит на эритроцитах к моменту рождения (Anderson и соавт. [1]). Исследования методом проточной цитофлюориметрии показали, что он отсутствует на лимфоцитах, нейтрофилах и моноцитах
Частота антигена Sc2 у различных народов
|
Популяция |
Количество обследованных |
Частота Sc2+ |
Источник |
|
|
абс. ч. |
% |
|||
|
Канадские доноры |
1000 |
1 |
од |
[3] |
|
Белые канадцы |
348 |
5 |
1,44 |
[1] |
|
Белые канадцы |
1000 |
17 |
1,70 |
[19] |
|
Канадские индейцы Манитоба |
100 |
[19] |
||
|
Канадские негры |
212 |
[17] |
||
|
Жители Лондона |
1039 |
7 |
0,67 |
[34] |
|
Доноры Оксфорда |
5306 |
41 |
0,77 |
[27] |
|
Доноры Варшавы |
1025 |
9 |
0,88 |
[34] |
|
Доноры Берлина |
2015 |
15 |
0,74 |
[10] |
|
Чешские доноры |
2100 |
7 |
0,33 |
[13] |
|
Эскимосы |
75 |
[19] |
||
|
Японцы |
4900 |
5 |
0,05 |
[25] |
|
Китайцы (Тайвань) |
161 |
[39] |
||
- Категория: Система Scianna и система Dombrock
Антиген Sc3 и нулевой фенотип Scnull
По описанию МсСгеагу и соавт. [22], пациенту Sc:—1,—2 с Маршалловых островов за 7 мес. до обследования перелили кровь. Как впоследствии стало ясно, фенотип этого человека был Sc:-l,-2,-3, или нулевой фенотип Scianna -Scnull. У пробанда имелись антитела, реагировавшие с эритроцитами всех членов семьи за исключением его собственных и эритроцитов его двоюродной сестры. Сестра матери больного также имела фенотип Sc:-l,-2,(-3), в то время как его родители и другие члены семьи были Sc: 1,-2,(3). В сыворотке крови упомянутой тети больного, имевшей четыре беременности, антитела анти-Sc отсутствовали.
У другого реципиента Sc:-l,-2, белого мужчины, имелись антитела, реагировавшие со всеми образцами эритроцитов, за исключением Sc:-l,-2,(-3) (Nason и соавт. [26]). Адсорбция - элюция сыворотки больного эритроцитами Sc:l,-2 и Sc:-1,2 показала, что антитела не являются смесью анти-Scl- и анти-8с2-антител, а представляют собой одно несепарируемое антитело, открывающее качественно новый антиген, который получил обозначение Sc3.
Третьим человеком Sc:-l,-2,-3, имевшим anra-Sc3-антитела, оказалась четырехлетняя девочка из Папуа - Новой Гвинеи, которой производили гемотрансфузии (Woodfield и соавт. [38]). Ее мать также имела фенотип Sc:-l,-2,-3. При обследовании 29 членов этой семьи и жителей селения, где она проживала, выявлены еще 6 человек, имевших фенотип Sc: -1,-2,-3, 2 из которых не являлись родственниками ребенка.
Антитела с высокой частотой реагирования найдены у 3 мужчин с фенотипом Sc:l,-2, которым производили гемотрансфузии. Указанные антитела не реагировали с эритроцитами Sc:-l,-2, а также с собственными эритроцитами обследованных (Devine и соавт. [7]). Вместе с тем они реагировали с эритроцитами других носителей антител анти-Sc, имевших фенотип Sc:l,-2. Исследования показали, что все три образца антител открывают отличающиеся друг от друга антигены. Один из образцов антител не реагировал с аутологичными эритроцитами и эритроцитами носителя антител с фенотипом Sc:l,-2. Два других образца реагировали с эритроцитами всех произвольно выбранных лиц. Попытки установить специфичность указанных антител успеха не имели (Daniels [5]).
Banks и соавт. [2] нашли антитела с высокой частотой реагирования у жителя Сенегала с фенотипом Sc:-l,-2. Антитела также не были идентифицированы, хотя и реагировали с эпитопами, расположенными на гликопротеине Scianna.
Антиген Sc4 (Radin, Rd, Rda)
Первые образцы антител к антигену Radin (Rd, Rda), получившему впоследствии обозначение Sc4, были выявлены Rausen и соавт. [32] у беременных. Sc4 относится к редко встречающимся антигенам (табл. 15.3). Ген Rd имеет аутосомно-доминантный характер наследования (Rausen и соавт. [32], Lundsgaard, Jensen [21], Lewis и соавт. [18], Race, Sanger [31]).
Таблица 15.3
Частота антигена Sc4 у различных народов
|
Популяция |
Количество |
Частота, % |
Источник |
|
|
обследованных |
Sc4+ |
|||
|
Смешанная |
6773 |
[32] |
||
|
Канадцы |
770 |
3 |
0,39 |
[18] |
|
Канадские индейцы Манитоба |
170 |
1 |
0,59 |
[18] |
|
Канадские доноры Виннипега |
2864 |
9 |
0,31 |
[18] |
|
Евреи, Нью-Йорк |
562 |
3 |
0,53 |
[32] |
|
Датчане |
4933 |
24 |
0,49 |
[21] |
Причиной образования антител aHTH-Sc4, как правило, была беременность или гемотрансфузия. В одном случае анти- 8с4-антитела имели естественное происхождение: они присутствовали у мужчины, которому не производили гемотрансфузии (Lundsgaard, Jensen [21]). При исследовании сывороток крови 30 000 датчан антитела aHra-Sc4 не найдены ни разу (Lundsgaard, Jensen [21]).
Предположение о том, что антиген Sc4 относится к системе Scianna, высказано Lewis и соавт. [18,20]. К этому времени было известно, что локусы Scianna и резус находятся на коротком плече хромосомы 1 (Noades et al [27]). Однако посемейные исследования показали, что антиген Sc4 наследуется независимо от антигенов резус и принадлежит системе Scianna (Lewis и соавт. [18,20]).
Методом иммуноблоттинга с использованием антител aHin-Sc4 было показа-1 (Spring [35]), что гликопротеин, несущий эпитопы Sc4, имеет мол. массу около 60 кДа, которая соответствует мол. массе гликопротеина Scianna. Гликопротеин, выделенный из эритроцитов Sc4+ с использованием антител анти-Sc 1, не реагировал с антителами airra-Sc4. Позднее были найдены лица с фенотипом Sc:l, 2,4, что позволило объяснить полученные Spring результаты: ген Rd (Sc4) не является аллельным по отношению к генам Sc1 и Sc2, в следствие чего антигенные эпитопы Scl/Sc2 и Sc4 расположены в различных участках гликопротеина Scianna
- Категория: Система Scianna и система Dombrock
Антигены Scianna расположены на гликопротеине, известном как HERMAP (human erythroid membarne associated protein - протеин, ассоциированный с мембраной эритроидных клеток человека). Синтез этого гликопротеина контролирует ген ERMAP, картированным на коротком плече хромосомы 1 в позиции 1р34.1. Ген ERMAP включает 11 экзонов протяженностью 19 пн.
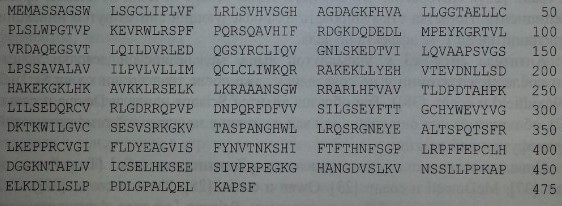
Протеин HERMAP состоит из 475 аминокислот (рис. 15.2) и представлен экстрацеллюлярным, трансмембранным и интрацеллюлярным доменами, включающими соответственно 157, 20 и 198 аминокислот
Последовательность протеина HERMAP
Молекулярная основа нулевого фенотипа Scianna разнородна (см. табл. 15.4). В результате мутаций или делеций генетического материала у лиц с нулевым фенотипом (Sc:-1,-2,-3) синтезируемый протеин HERMAP утрачивает антигенные эпитопы, распознаваемые антителами Scianna. Фенотипически это проявляется в отсутствии всех без исключения антигенов указанной системы. Как уже отмечено выше, лица с фенотипом Sc „ могут быть аллоиммунизированы часто встречающимся антигеном Sc3.
- Категория: Система Scianna и система Dombrock
Антигены Sc5, Sc6 и Sc7
Антитела, полученные от лиц с нулевым фенотипом Sc:-l,-2,-3, и фенотипами Sc:—1,2, 3 и Sc:l,-2,3, проявляли очевидную гетерогенность и перекрестную реактивность с эритроцитами разных фенотипов, в том числе трех перечисленных. Выявляемые с помощью этих антител антигены различались между собой. Усилиями молекулярных генетиков удалось установить, что все лица, выработавшие антитела к антигенам Scianna, были гомозиготами по точковым мутациям в разных участках гена ERMAP (табл. 15.4) (Flegel и соавт. [9] и Hue-Roye и соавт. [12]. Таким образом, система Scianna пополнилась сразу тремя антигенами.
Данные о клиническом значении антител affra-Sc5, airra-Sc6 и amn-Sc7 в литературе не представлены.
Свойства
Антигены Scianna устойчивы к действию большинства протеолитических ферментов, используемых в иммуносерологии: папаина, трипсина, бромели-на, химотрипсина (Daniels [4]). Обработка эритроцитов проназой, а также смесью трипсина и химотрипсина уменьшает выраженность этих антигенов. Резкое снижение экспрессии антигенов Scl и Sc2 отмечалось после обработки эритроцитов сульфгидрильными редуцентами (Spring и соавт. [36]). Это свидетельствовало о присутствии в структуре антигенов Scianna одной или более дисуль-фидных связей. Эндогликозилаза F, расщепляющая JV-гликаны, несколько угнетала связывание антител анти-Sc 1 с соответствующим антигеном. При этом связывание антител amn-Sc2 полностью устранялось. По-видимому, аминокислотная замена, определяющая специфичность антигенов Scl и Sc2, каким-то образом связана с iV-гликозилированием протеина Scianna. Обработка эритроцитов сиалидазой уменьшала мол. массу гликопротеина Scianna, изменяла его элек-трофоретическую подвижность.
Антитела системы Scianna
Антитела к антигенам Scianna встречаются редко. Они представлены, как правило, иммуноглобулинами G, лучше выявляются в антиглобулиновой пробе, не связывают комплемент. Описаны агглютинирующие антитела системы Scianna.
Четыре образца анти-8с2-антител выявлены у доноров - добровольцев, иммунизированных с целью получения реактивов анти-D. Один из доноров, эритроциты которого использовали для иммунизации, имел фенотип D+Sc2+ (Seyfried и соавт. [34]).
По данным Mollison и соавт. [24], из 19 добровольцев с фенотипом D-Sc2-, получивших по две и более инъекции эритроцитов D+Sc2+, у 8 образовались анти-Б-антитела и только у одного - анти-8с2-антитела.
В пяти случаях анти-8с4-антитела вызвали легкую форму ГБН, только одному из новорожденных потребовалось обменное переливание крови (Rausen и соавт. [32]).
DeMarco и соавт. [6] привели описание одного случая легкой формы ГБН, обусловленной анти-8с2-антителами.
В другом случае у новорожденного была зарегистрирована положительная прямая проба Кумбса, обусловленная антителами анти-Sc 1 субкласса IgG3, однако проведения лечебных мероприятий при этом не потребовалось (Кауе и соавт. [14]).
Антитела системы Scianna не вызывали гемолитических осложнений после гемотрансфузии. Однако исследование приживаемости радиоактивно меченных эритроцитов в организме больного, имеющего антитела анти-8сЗ, показало относительно быстрое выведение эритроцитов из кровяного русла (МсСгеагу и соавт. [22]). Интересно, что антитела также вскоре исчезли из плазмы крови реципиента. Попытка стимулировать их последующий синтез путем инъекции эритроцитов Sc:l,-2 эффекта не дала.
Антитела анти-8сЗ у упомянутой выше меланезийской девочки исчезли после спленэктомии и не появлялись даже после трансфузии крови Sc:l,-2 (Woodfield и соавт. [38]). Три образца антител Scianna описали Devine и соавт. [7], об одном из них они сообщили как о причине замедленной гемолитической трансфузионной реакции.
Описано несколько случаев выявления аутоантител анти-Sc 1 (Tregellas и соавт. [37], McDowell и соавт. [23], Owen и соавт. [28], Pierse и соавт. [30]). У 2 больных, имевших ослабленные антигены Scianna, помимо фиксированных на эритроцитах аутоантител, присутствовали свободно циркулирующие аутоантитела, которые находили в сыворотке крови, но не обнаруживали в плазме (McDowell и соавт. [23]).
У одного ребенка аутоиммунная гемолитическая анемия, вызванная аутоанти-телами анти-Sc 1, не поддавалась лечению кортикостероидами. Положительный лечебный эффект получен только после удаления селезенки (Owen и соавт. [28]).
Peloquin и соавт. [29] выявили аутоантитела aHTH-Sc3 в сыворотке крови 2 больных (с лимфомой и болезнью Ходжкина). Экспрессия антигенов Scl и Sc3 на их эритроцитах была снижена. Аутоантитела реагировали слабее с эритроцитами Sc:-1,2, чем Sc:l,-2.
- Категория: Система Scianna и система Dombrock
До 1995 г. к системе Dombrock (Домброк) относили два антитетичных антигена - DoaH Dob. В 1995 г. Banks и соавт. [1] установили, что у лиц, лишенных антигенов Do8 и Dob, отсутствуют также еще три антигена - Gya, Ну и Joa - и они имеют фенотип Do(a-b-)Gy(a-)Hy-Jo(a-). Столь очевидная фенотипи-ческая связь позволила расширить систему Dombrock до пяти единиц. В нее были включены часто встречающиеся антигены Gya (Gregory), Ну (Holley) и Joa(Joseph), получившие обозначения D03, D04 и D05 в номенклатуре ISBT. Антигены DoaH Dob получили обозначения D01 и D02 (табл. 16.1).
Таблица 16.1
Антигены Dombrock
|
Обозначение |
Частота среди европеоидов, % |
Примечание |
|
|
традиционное |
ISBT |
||
|
Doa (Dombrock) |
DOl |
66 |
Антитетичен антигену Do , замена Asn 265 |
|
Dob |
D02 |
82 |
Антитетичен антигену Doa, замена Asp 265 |
|
Gya (Gregory) |
D03 |
>99 |
Отсутствует на эритроцитах лиц Do(a-b-) |
|
Ну (Holley) |
D04 |
>99 |
Отсутствие антигена Ну обусловлено заменами Gly 108 Val и Leu 300 Val, при этом антигены Dob и Gya слабо выражены |
|
Joa (Joseph) |
D05 |
>99 |
Отсутствует на эритроцитах Ну- |
|
DOYA |
D06 |
|
См. гл. 37 |
Антигены Doa, Dob и Joa полностью развиты к моменту рождения (Swanson и соавт. [45], Molthan и соавт. [23], Laird-Fryer и соавт. [18], Jensen и соавт. [14]). Антигены Gya и Ну, наоборот, на эритроцитах новорожденных выражены слабо (Clark и соавт. [6], Moulds и соавт. [26]).
Обработка эритроцитов папаином или фицином повышает серологическую активность антигенов Dombrock, поэтому антиглобулиновый тест с клетками, предварительно обработанными указанными ферментами, является оптимальным, особенно при определении антигенов Doa и Dob.
Вещество Dombrock разрушается трипсином, химотрипсином, проназой и сульфгидрильными редуцентами. Сиалидаза подобного эффекта не оказывает (Banks и соавт. [1], Brown [4], Spring и соавт. [42,43]).
Антигены Dombrock расположены на гликопротеине, связанном с гликозил-фосфадитилинозитолом (ГФИ). Этот пептид относится к группе аденозинди-фосфатрибозилтрансфераз.
Генный локус DO картирован на хромосоме 12 в позиции 12р13.2-12.1
Doa и Dob
В 1965 г. Swanson и соавт. [45] обнаружили у европейки по фамилии Dombrock антитела, реагирующие с эритроцитами примерно 64 % произвольно выбранных доноров. Авторы показали, что антиген, обозначенный ими Doa, не связан с другими антигенами эритроцитов и может быть отнесен к новой, ранее неизвестной системе.
В 1973 г. Molthan и соавт. [23] нашли антитела, открывающие антитетичный антиген - Dob.
Данные о частоте антигенов Dombrock у различных народов неполны, поскольку получены, в основном, с использованием сывороток анти-Ооа. Чаще всего антиген Doa встречается у европеоидов и негроидов, реже - у монголоидов (табл. 16.2, 16.3). Полученная на основе этих данных расчетная частота генотипов Do a/Do а, Do a/Do bnDo b/Dob составила соответственно 0,1764; 0,4872 и 0,3364.
Таблица 16.2
Частота антигена Doa и генов Doa и Dob у разных народов
|
Популяция |
Количество обследованных |
Частота антигена Doa |
Частота генов |
Источник |
||
|
абс. ч. |
% |
Do" |
Dob |
|||
|
Жители стран Северной Европы |
755 |
501 |
66,36 |
0,4200 |
0,5800 |
[45,48, 49] |
|
Белые американцы |
391 |
250 |
63,94 |
0,3395 |
0,6005 |
[30] |
|
Жители стран Северной Америки |
700 |
446 |
63,71 |
0,3976 |
0,6024 |
[19] |
|
Американские негры |
161 |
89 |
55,28 |
0,3313 |
0,6687 |
[30] |
|
Американские негры |
76 |
34 |
44,74 |
0,2566 |
0,7434 |
[48] |
|
Японцы |
760 |
179 |
23,55 |
0,1257 |
0,8743 |
[27,28] |
|
Жители Таиланда |
423 |
57 |
13,48 |
0,0698 |
0,9302 |
[5] |
Исследование эритроцитов более 2500 членов канадских, израильских, японских, негритянских и других семей с помощью сывороток анти-Ооа показало, что во всех случаях независимо от расовой принадлежности ген Doa проявлял себя как аутосомно-доминантный признак (Tippett и соавт. [48, 49], Lewis и соавт. [19], Polesky, Swanson [30]). У родителей Do(a+) х Do(a-) частота ожидаемых и частота фактических фенотипов детей по антигену Doa совпадали.
Частота фенотипов Dombrock
|
Сочетание антигенов |
Частота (%) среди |
|||||
|
Doa |
Dob |
Gya |
Ну |
Joa |
европеоидов |
негроидов |
|
+ |
— |
+ |
+ |
+ |
18 |
11 |
|
+ |
|
+ |
1 |
+ |
49 |
44 |
|
— |
| |
+ |
+ |
+ |
33 |
45 |
|
— |
— |
— |
|
— |
Редко |
|
|
— |
сл |
сл |
— |
— |
Редко |
|
|
сл |
сл |
+ |
сл |
— |
Редко |
|
Примечание: « + » - антиген присутствует; « - » - антиген отсутствует; сл - антиген слабо выражен.
Gy-
В другой семье, также чешского происхождения, было две женщины Gy(a-), содержавшие анти-Оуа-антитела. Обе женщины имели повторные беременности (Race, Sanger [32]).
Еще 6 индивидов Gy(a-) выявлены в английской семье, имевшей, как полагают Clark и соавт. [6], романское происхождение. У 4 сестер обнаружены анти-Оуа-антитела, у 2 их братьев они отсутствовали. Сестры имели многократные беременности.
Okubo и соавт. [29] описали 6 японских женщин Gy(a-). Редкий фенотип выявлен в связи с обнаружением у них анти-Оуа-антител.
Мак и соавт. [20] наблюдали мужчину Gy(a-) (китайца из Гонконга), имевшего анти-Gyа-антитела, вероятно, аллоиммунной природы: 40 лет назад ему перелили кровь.
Антиген Gya присутствует практически у всех людей. Лица Gy(a-) не были обнаружены при обследовании 9350 японцев (Okubo и соавт. [29]) и 10 145 американцев (Swanson и соавт. [46]). Среди негроидов Фенотип Gy(a-) не выявлен.
Из большого числа обследованных (4530 белых американцев, 735 чехов, 683 белых южноафриканца, 846 американских негров, 1023 черных южноафриканца, 633 южноафриканских индуса, 1679 американских индейцев) только один человек - европеец по происхождению - имел фенотип Gy(a-) и два индейца племени апачи имели фенотип Gy(a+W). Остальные обследованные были Gy(a+).
Ген, формирующий фенотип Gy(a-), наследуется по рецессивному типу. Описаны супружеские пары Gy(a+) х Gy(a+), имевшие детей Gy(a-) (Swanson и соавт. [46], Clark и соавт. [6], Okubo и соавт. [29], Massaquoi [21]). Родители, как правило, были кровными родственниками (Swanson и соавт. [46], Okubo и соавт. [29], Massaquoi [21]).
На эритроцитах Gy(a-) отсутствуют антигены Ну и Joa (Moulds и соавт. [26], Laird-Fryer и соавт. [18]), а также Doa и Dob. Подобная фенотипическая зависимость указывала на то, что перечисленные антигены могут входить в одну систему.
Ну
Первый образец сыворотки, содержащей анти-Ну-антитела, получили Schmidt и соавт. [40]. Позднее были найдены другие образцы антител указанной специфичности (Moulds и соавт. [26], Beattie, Castillo [3], Hsu и соавт. [12]). Носителями антител во всех случаях были негроиды, имевшие фенотип Ну-.
Moulds и соавт. [26] отметили фенотипическую связь антигенов Ну и Gya. Негроиды Ну- имели слабый антиген Gya [фенотип Hy-Gy(a+W)], тогда как у европеоидов Ну- и монголоидов Ну- антиген Gya отсутствовал.
Индивиды Hy-Gy(a-) вырабатывали анти-Gyа-антитела, индивиды Hy-Gy(a+W) - анти-Ну-антитела.
Сыворотки aHTH-Gya не содержали антител анти-Ну. Троекратная адсорбция сывороток aHTH-Gya эритроцитами Hy-Gy(a+W) полностью истощала активность анти-Оуа-антител. Элюаты с указанных эритроцитов вели себя в серологических реакциях так же, как антитела исходных неадсорбированных сывороток aHTH-Gya.
Все лица Hy-Gy(a+W) были Do(a-b+w), антиген Doay них отсутствовал, антиген Dob был выражен слабо (Banks и соавт. [1]).
У 7 лиц Hy-Gy(a+W), обследованных с использованием молекулярно-биологических методов, была найдена замена нуклеотида G 232 Т в экзоне 2, ведущая к аминокислотной замене Gly 108 Val (Rios и соавт. [37, 38]). У указанных индивидов обнаружена мутация С 898 G в экзоне 3, которая приводила к аминокислотной замене Leu 300 Val и, соответственно, уменьшала экспрессию антигенов Gya и Dob.
Joa
О выявлении антигена Joa (Joseph) впервые сообщили Jensen и соавт. [14], которые нашли антитела, идентифицировавшие этот антиген у 2 пациентов -американских негров. Обе сыворотки реагировали со всеми исследованными эритроцитами.
Третий образец анти^оа-антител обнаружили Morel и соавт. [24] у больного с серповидно-клеточной анемией.
Все три носителя анти^оа-антител получали многократные гемотрансфузии.
Laird-Fryer и соавт. [18] выявили у 5 негритянок антитела, обозначенные как aHTH-Jca. Позднее было показано, что эти антитела и антитела анти-Joа реагируют с одним и тем же антигеном (Weaver и соавт. [52]).
Частота встречаемости антигена Joa очень высока. Jensen и соавт. [14] при обследовании 3000 жителей Нью-Йорка, преимущественно европеоидов, а также 7689 американских негров не нашли ни одного человека с фенотипом Jo(a-).
Позднее было установлено, что антиген Joa отсутствует на эритроцитах лиц Hy-Gy(a-) и Hy-Gy(a+W), что свидетельствовало о фенотипической связи этих антигенов и возможной принадлежности к одной групповой системе. Вместе с тем все лица, имевшие анти-1оа-антитела, были Gy(a+)Hy+Jo(a-) (Laird-Fryer и соавт. [18], Weaver и соавт. [51], Brown и соавт. [4]). Тем самым было показано, что антигены Gya, Ну и Joa полностью различаются между собой.
Антиген Ну несколько отличался от антигена Joa. Если антиген Joa отсутствовал на эритроцитах Hy-Gy(a-) и обнаруживался только на эритроцитах Hy+Gy(a+), то антиген Ну присутствовал на эритроцитах и Gy(a+)Jo(a+), и Gy(a+) Jo(a-) (Spring и соавт. [43]).
Weaver и соавт. [51] нашли 4 человек Hy-Gy(a-)Jo(a-). Banks и соавт. [1] выявили пять человек Jo(a-)Do(a+wb+w) негров, одного испанца Jo(a-)Do(a+wb-).